
【题目】A、B、C、D、E、F、G、H八种主族元素分布在三个不同的短周期,它们在周期表中位置如下:
A | ||||||
B | C[ | D | ||||
E | F | G | H | |||
请回答下列问题:
(1)写出E元素在周期表中的位置 。
(2)B与D可形成三原子分子X,X的电子式为 。
(3)E、F、H所形成的简单离子的半径由大到小的顺序为 (用离子符号表示)。
(4)G的最高价氧化物与B的单质在高温下能发生置换反应,其化学反应方程式为:
。
(5)由A、C、D三种元素组成的强电解质Z溶于水时能促进水的电离,测得Z的水溶液pH<7,其原因是 (用离子方程式来表示)。
(6)盐Y由B、D、E组成。以熔融盐Y为电解质构成的燃料电池如图所示。
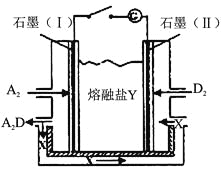
写出石墨(I)电极上发生的电极反应式 。
(7)用熔融盐Y的燃料电池作电源,以石墨为电极,电解一定浓度的CuSO4溶液至无色后继续电解一段时间。断开电路,向溶液中加入0.1 mol Cu(OH)2,溶液恢复到电解之前的体积和浓度,则电解过程中转移电子的物质的量为 。
【答案】(1)第三周期第IA族
(2)![]()
(3)r(S2-)>r(Na+)>r(Al3+)
(4)SiO2+2C高温 Si+2CO↑
(5)NH4+ + H2O![]() NH3·H2O+H+
NH3·H2O+H+
(6)H2+![]() -2e-=H2O+CO2
-2e-=H2O+CO2
(7)0.4mol
【解析】试题解析:A、B、C、D、E、F、G、H八种元素分布在三个不同的短周期,由元素再周期表中位置,可知A为H元素;B为碳元素,C为N元素;D为O元素;E为Na,F为Al;G为Si;H为S元素。
(1)E为钠元素,它在周期表中的位置是第三周期第IA族。
(2)B与D形成的三原子分子X是CO2,其电子式为![]() 。
。
(3)电子层结构相同的离子,核电荷数越大离子半径越小,电子层数越多离子半径越大,故离子半径:S2-
>Na+>Al3+。
(4)G的最高价氧化物为SiO2,与B的单质(碳)在高温下能发生置换反应,其化学反应方程式为:SiO2+2C
![]() Si+2CO↑。
Si+2CO↑。
(5)由H、N、O三种元素组成的强电解质Z溶于水时能促进水的电离,测得Z的水溶液pH<7,则Z为
NH4NO3,溶液中由于铵根离子水解使溶液呈酸性:NH4++H2ONH3H2O+H+。
(6)盐Y由C、O、Na组成,则Y为Na2CO3,以熔融盐Na2CO3为电解质、氢气、氧气构成的燃料电池,
由图可知石墨(I)是氢气失去电子,与碳酸根离子结合生成水与二氧化碳,电极反应式:H2+![]() -2e-=
-2e-=
H2O+CO2。
(7)电解发生反应:2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,2H2O
2Cu+O2↑+2H2SO4,2H2O![]() 2H2↑+O2↑,相当于从溶液中析出
2H2↑+O2↑,相当于从溶液中析出
CuO、失去部分水,向溶液中加入0.1mol Cu(OH)2,溶液恢复到电解之前的体积和浓度,将Cu(OH)2
可以改写为CuOH2O,电解中生成Cu为0.1mol,2H2O![]() 2H2↑+O2↑中电解的水为0.1mol,整个
2H2↑+O2↑中电解的水为0.1mol,整个
过程转移电子为0.1mol×2+0.1mol×2=0.4mol。


科目:高中化学 来源: 题型:
【题目】仔细分析如图装置,完成下面的填空:
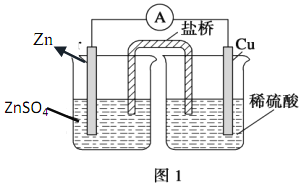
(1)该反应的电流方向是_____________。
(2)盐桥中的阴离子向________溶液中移动。
(3)一段时间后,锌片上的现象是_____________,铜片上的现象是______________。
(4)锌极发生_________反应,总反应方程式为_________________。
(5)30min后,1.3g的Zn参加了反应,则转移了_______个电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来各国都在寻找对环境无害而作用快速的消毒剂,其中二氧化氯(ClO2)是目前国际上倍受瞩目的第四代高效、无毒的消毒剂。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某兴趣小组的学生设计了如下模拟装置来制取、收集ClO2并测定其质量。
查阅资料:ClO2是一种黄红色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,温度过高可能引起爆炸,易溶于水,易与碱液反应。
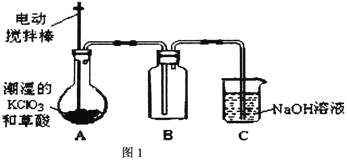
实验Ⅰ:制取并收集ClO2,如图1装置所示。
(1)装置A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式__________。
(2)装置A必须添加温度控制装置,其温度要保持在60~80℃之间,控制温度的目的是__________。装置B也必须添加温度控制装置,应该是__________(填“冰水浴”或“沸水浴”或“60℃的热水浴”)装置。
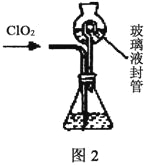
实验Ⅱ:测定ClO2质量,如图2装置所示。过程如下:
在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;按照图2组装好仪器;在玻璃液封管中加入水,浸没导管口;将生成的ClO2气体由导管通入锥形瓶的溶液中充分吸收后,把玻璃液封管中的水封液倒入锥形瓶中,再向锥形瓶中加入几滴淀粉溶液:用cmol/L硫代硫酸钠标准液滴定锥形瓶中的液体,共用去VmL硫代硫酸钠溶液(己知:I2+2S2O32-=2I-+S4O62-)。
(3)装置中玻璃液封管的作用是____________________。
(4)滴定终点的现象是____________________。
(5)测得通入ClO2的质量m(ClO2)=__________g(用整理过的含c、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是稀硫酸与某金属反应的实验数据:
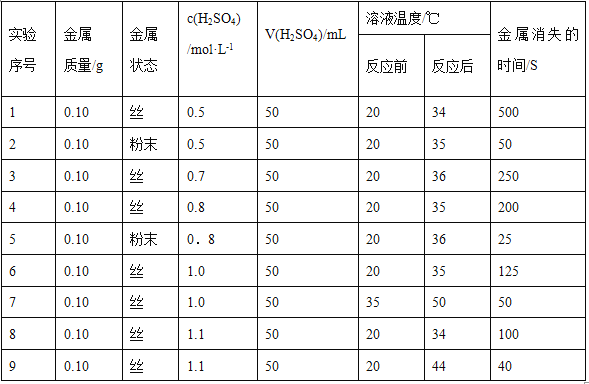
分析上述数据,回答下列问题:
(1) 实验4和5表明_________对反应速率有影响;________,反应速率越快,能表明这一规
律另一组实验是___________(填实验序号)。
(2) 在前4次实验中,能表明反应物浓度对反应速率产生影响的实验有____(填序号)。
(3) 本实验中影响反应速率的其他因素还有_________,其实验序号是_____。
(4) 实验中,反应前后溶液的温度变化值(约15℃)相近,推测其原因:
_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇可以补充和部分替代石油燃料,缓解能源紧张。利用CO可以合成甲醇。
(1)已知:CO(g)+![]() O(g)=CO2(g) △H1=-283.0kJ·mol-1
O(g)=CO2(g) △H1=-283.0kJ·mol-1
H2(g)+ ![]() O2(g)=H2O(l) △H2=-285.8kJ·mol-1
O2(g)=H2O(l) △H2=-285.8kJ·mol-1
CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(l) △H3=-764.5kJ·mol-1
O2(g)=CO2(g)+2H2O(l) △H3=-764.5kJ·mol-1
则CO(g)+2H2(g)=CH3OH(g) △H=__________kJ·mol-1
(2)甲图是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到达平衡,用H2表示平均反应速率v(H2)=____________________。

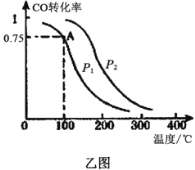
(3)一定条件下,在容积为VL的密闭容器中充入amolCO与2amolH2合成甲醇,平衡转化率与温度、压强的关系如乙图所示。
①P1__________P2(填“>”、“<”或“=”)
②该甲醇合成反应在A点的平衡常数K=__________(用a和V表示)
③下列措施中能够同时满足增大反应速率和提高CO转化率的是__________。(填写相应字母)
A.使用高效催化剂B.降低反应温度
C.增大体系压强D.不断将CH3OH从反应混合物中分离出来
E.向体系中再充入amolCO与2amolH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )
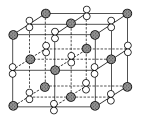
A. 与K+最近且距离相等的K+有6个
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
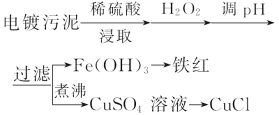
【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.3 | 7.6 | 4.4 |
完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是 。调pH步骤中加入的试剂最好是 (填化学式)。实验室进行过滤操作所用到的玻璃仪器有 、 、 。
(2)煮沸CuSO4溶液的原因是 。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式 。
(3)Fe3+发生水解反应Fe3++3H2O![]() Fe(OH)3+3H+,该反应的平衡常数表达式为 。
Fe(OH)3+3H+,该反应的平衡常数表达式为 。
(4)称取所制备的CuCl样品0.250 0 g置于一定量的0.5 mol·L-1FeCl3溶液中,待样品完全溶解后,加水20 mL,用0.100 0 mol·L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00 mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乳酸的结构简式为 。试回答:
。试回答:
(1)乳酸分子中含有________和_________两种官能团(写名称)。
(2)乳酸与金属钠反应的化学方程式为______________________________________________。
(3)乳酸与Na2CO3溶液反应的化学方程式为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——物质结构与性质】
氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)基态N原子中电子在2p轨道上的排布遵循的原则是________。前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为__________________。
(2)C、N、O三种元素第一电离能从大到小的顺序是__________________________
(3)N2F2分子中N原子的杂化方式是___________________,l mol N2F2含有______mol![]() 键。
键。
(4)NF3的键角______NH3的键角(填“<”“>”或“=”),原因是__________________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。l mol NH4BF4_________mol配位键。
(6)安全气囊的设计原理为6NaN3+FeIO3![]() Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑

①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质。写出两种与N3-互为等电子体的分子或离子____________。
②Na2O的晶胞结构如图所示,品胞边长为566pm,晶胞中氧原子的配位数为_____,Na2O晶体的密度为_____g·cm-3(只要求列算式,不必计算出结果)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com