
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
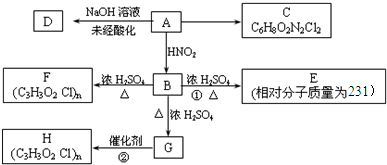






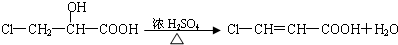

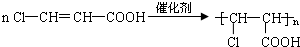
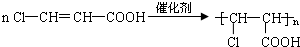
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
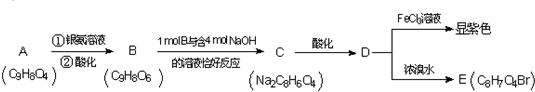





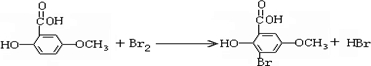

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
(13分)某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究。回答下列问题:
(1)图中D装置在实验中的作用是 。
(2)从以下所给物质中选出甲同学设计的实验所用到物质:
图1中试剂A为_________;试剂C为_________(填序号)。
①稀HNO3溶液②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2i
写出烧瓶中发生反应的离子方程式____________________。
写出试管C中发生反应的离子方程式___________________________。
由此判断,元素N、C、Si 非金属性由弱到强的顺序为___________。
(3) 乙同学设计的实验所用到试剂A为________;试剂B为________;试剂C为________。
C处的现象为浅黄色沉淀产生;写出C中发生反应的化学方程式为 ___ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com