
����Ŀ����Ԫ������Ȼ����Ҫ�����ᣮ�����κ�������δ��ڣ���ش��������⣺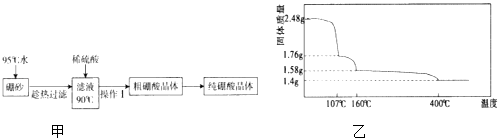
��1����Ԫ���Ǣ�A��ĵ�һ��Ԫ�أ�ԭ�ӽṹʾ��ͼΪ �� ��Ȼ��Ԫ���������ȶ�ͬλ��10B��11B�������ԭ�������ֱ�Ϊ10��11�����ǵ���Է�ȷֱ�Ϊ20%��80%����Ԫ�ص�ƽ���������Ϊ ��
��2�����ᣨH3BO3����һԪ���ᣬ��ҵ������ɰ��Na2B4O710H2O���Ʊ����ᾧ���������ͼ�ף�
��ͬ�¶���������ܽ�ȼ��±���
�¶�/�� | 0 | 20 | 40 | 60 | 80 |
�ܽ��/g | 2.7 | 5.0 | 8.7 | 14.8 | 23.8 |
��д����ɰ��Һ��ϡ���ᷴӦ�����ӷ���ʽ ��
�����������л�ô����ᾧ��IJ�����Ϊ�����ˣ���һ���������ᾧ���ᴿ�ķ����� ��
��25��ʱ0.1mol/L������Һ��pHԼΪ5.1��������볣��KԼΪ ��
��3�������ڼ��ȹ����з����ֽ��ʧ��������ͼ����ʾ��
������ӿ�ʼ���ȵ�107��ʱ��������Ӧ�Ļ�ѧ����ʽΪ ��
��������ȵ�160��õ��Ĺ���Ļ�ѧʽΪ �� ��BԪ�ص����ԭ��������11���㣩
��4��NaBH4����HԪ���ԩ�1�ۣ�����ǿ��ԭ�ԣ����л���ѧ�ϵ����ܻ�ԭ�����ڼ��������µ��NaBO2��Һ�����Ƶ�NaBH4 �� �䷴Ӧ����ʽΪNaBO2+2H2O=2O2��+NaBH4 �� ��������ӦʽΪ ��
���𰸡�
��1��![]() ��10.8
��10.8
��2��5H2O+B4O72��+2H+=4H3BO3�����½ᾧ����ȴ�ȱ�����Һ�����ؽᾧ��10��9.2
��3��H3BO3�THBO2+H2O��H2B4O7
��4��BO2��+6H2O+8e��=BH4��+8OH��
���������⣺��1����ĺ˵����=�����������=5����ԭ�ӽṹʾ��ͼΪ�� ![]() ����Ȼ��Ԫ���������ȶ�ͬλ��10B��11B�������ԭ�������ֱ�Ϊ10��11�����ǵ���Է�ȷֱ�Ϊ20%��80%������Ԫ�ص�ƽ���������Ϊ��10��20%+11��80%=10.8��
����Ȼ��Ԫ���������ȶ�ͬλ��10B��11B�������ԭ�������ֱ�Ϊ10��11�����ǵ���Է�ȷֱ�Ϊ20%��80%������Ԫ�ص�ƽ���������Ϊ��10��20%+11��80%=10.8��
���Դ��ǣ� ![]() �� 10.8����2������ɰ��Һ������ΪNa2B4O710H2O����ϡ���ᷴӦ����H3BO3�������ƣ���Ӧ�����ӷ���ʽΪ��5H2O+B4O72��+2H+=4H3BO3 ��
�� 10.8����2������ɰ��Һ������ΪNa2B4O710H2O����ϡ���ᷴӦ����H3BO3�������ƣ���Ӧ�����ӷ���ʽΪ��5H2O+B4O72��+2H+=4H3BO3 ��
���Դ��ǣ�5H2O+B4O72��+2H+=4H3BO3�� �ڸ��ݱ���������ܽ�ȿ�֪���������¶ȵ�Ӱ��ϴ���ͨ�������¶ȵķ�����������ᣬ�����������л�ô����ᾧ��IJ�����Ϊ���½ᾧ����ȴ�ȱ�����Һ�������ˣ�����һ���������ᾧ���ᴿ������ͨ���ؽᾧ�ķ�����ɣ����Դ��ǣ����½ᾧ����ȴ�ȱ�����Һ�����ؽᾧ����25��ʱ0.1mol/L������Һ��pHԼΪ5.1�������Һ��������Ũ��Ϊ��c��H+��=10��5.1mol/L��c��H2BO3������c��H+��=10��5.1mol/L����������ĵ���̶Ƚ�С����0.1mol/L������Һ��δ���������Ũ��ԼΪ0.1mol/L����������ĵ���ƽ�ⳣ��Ϊ��K= ![]() =10��9.2 �� ���Դ��ǣ�10��9.2����3����2.48g��������ʵ���Ϊ��
=10��9.2 �� ���Դ��ǣ�10��9.2����3����2.48g��������ʵ���Ϊ�� ![]() =0.04mol��107��ʱ���ٵĹ�������Ϊ��2.48g��1.76g=0.72g�����ٲ���Ӧ��Ϊˮ�����������ٵ�ˮ�����ʵ���Ϊ��
=0.04mol��107��ʱ���ٵĹ�������Ϊ��2.48g��1.76g=0.72g�����ٲ���Ӧ��Ϊˮ�����������ٵ�ˮ�����ʵ���Ϊ�� ![]() =0.04mol����1��������ʧȥ1����ˮ�����Ըù����з�Ӧ�ķ���ʽΪ��H3BO3�THBO2+H2O��
=0.04mol����1��������ʧȥ1����ˮ�����Ըù����з�Ӧ�ķ���ʽΪ��H3BO3�THBO2+H2O��
���Դ��ǣ�H3BO3�THBO2+H2O����ʣ������107����ȵ�160��ʱ������ˮ������Ϊ��1.76g��1.58g=0.18g�������ʵ���Ϊ�� ![]() =0.01mol��0.04mol HBO2�к���0.04molH��0.04molB��0.08molO��ʧȥ0.01molˮ��õ��Ĺ����к��У�0.02molH��0.04molB��0.07molO����H��B��Oԭ����֮��Ϊ��2��4��7����Ӧ�����Ļ�ѧʽΪ��H2B4O7 ��
=0.01mol��0.04mol HBO2�к���0.04molH��0.04molB��0.08molO��ʧȥ0.01molˮ��õ��Ĺ����к��У�0.02molH��0.04molB��0.07molO����H��B��Oԭ����֮��Ϊ��2��4��7����Ӧ�����Ļ�ѧʽΪ��H2B4O7 ��
���Դ��ǣ�H2B4O7����4���ܷ�ӦΪNaBO2+2H2O=2O2��+NaBH4 �� ����������������������Ӧ������������ԭ��Ӧ��������H2O�õ�������BO2���������BH4�������������ӣ������ĵ缫��ӦʽΪ��BO2��+6H2O+8e��=BH4��+8OH�� �� ���Դ��ǣ�BO2��+6H2O+8e��=BH4��+8OH�� ��


 ���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ��Ϊ2.00mol/L��������Һ1L����ʹ��Ũ�ȱ�Ϊ4.00mol/L�����з������е��ǣ� ��
A.������0.5Lˮ
B.�����ͨ��44.8L HCl����
C.����Һ��������Ũ����0.5L
D.����10mol/L����0.6L���ٽ���Һϡ����2L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����˶�Ա������˻�Ť��ʱ����ҽ�漴���˶�Ա�����˲�λ����ҩ��������(�е�Ϊ12.27��)���оֲ��䶳����Ӧ�����������й����������˵���в���ȷ����(����)
A.��������ˮ��������
B.�������к������ֹ�����
C.��������һ���������ܷ�����ȥ��Ӧ
D.������Ľṹֻ��һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�������ǣ� ��
A. ������ζ�������ˮ��������������еĵ����ʡ�3��
B. NH4Cl��NaCl���������������������
C. ��������������ȷֽ�IJ����о���NH3
D. NH4Cl��Һ�м���NaOHŨ��Һ���ȣ���Ӧ�����ӷ���ʽΪ NH4++OH- ==NH3��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��P�ǿ�����ƽ�л����Ļ���������ͬ�¶�ʱ����A�����г���2 mol SO3(g)���ر�K����B�����г���1 mol SO3(g)���������ֱ�����Ӧ��2SO3(g) ![]() 2SO2(g)+O2(g)����֪��ʼʱ����A��B�������Ϊa L���Իش�
2SO2(g)+O2(g)����֪��ʼʱ����A��B�������Ϊa L���Իش�
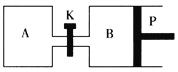
��1����Ӧ�ﵽƽ��ʱ����B�������Ϊ1.2aL������B��SO3ת����Ϊ___________��
��2������K��һ��ʱ������´ﵽƽ�⣬����B�����Ϊ___________L����ͨ��������������Բ�������
��3������ͬ���ʵ�����H2O(g)�� CO�ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У�������Ӧ��H2O(g)+CO��g��![]() CO2(g)+H2(g) ��H���õ��������ݣ�
CO2(g)+H2(g) ��H���õ��������ݣ�
ʵ�� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
H2O | CO | CO | H2 | |||
�� | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
�� | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
�� | 900 | 2 | 1 | a | b | t |
���ɱ������ݿ�֪�÷�Ӧ����H_______ 0������>������<������
��ʵ������a=______����ƽ��ʱʵ������ʵ������H2O(g)��ת���ʵĴ�С��ϵΪ����2(H2O)____��3(H2O)������>������<������=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����м���������ij���ӵIJ��������۲��������ǣ� ��
A.�ȼ�HCl�����������ټ�BaCl2�а�ɫ������һ����SO ![]()
B.����ϡ���������ʹ����ʯ��ˮ����ǵ���ζ���壬����Һ��һ����CO ![]()
C.��������������Һ�����ȣ�������������ʹʪ���ɫʯ����ֽ������һ����NH ![]()
D.����ɫ��Ӧ��ĩ�۲쵽��ɫΪ��ɫ�������Һ��һ�������м�Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����е�����������Ҫ��Ⱦ�Ϊ��������Ⱦ����ͨ��NH3 �� ������ӦNOx+NH3��N2+H2O��������Ⱦ������NO��NO2�Ļ������3L����ͬ��ͬѹ��3.5LNH3ʹ��ǡ����ȫת��ΪN2 �� ����������NO��NO2�����ʵ���֮��Ϊ�� ��
A.1��1
B.2��1
C.1��3
D.1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ2L���ܱ������з�����ӦxA��g����yB��g��![]() zC��g����ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ�¶�100����200��ƽ��ʱC�������������ʼn��A����n��B���ı仯��ϵ�������н�����ȷ����(����)
zC��g����ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ�¶�100����200��ƽ��ʱC�������������ʼn��A����n��B���ı仯��ϵ�������н�����ȷ����(����)
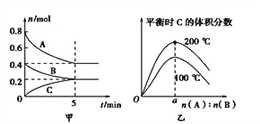
A. 200��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v��B����0.04 mol��L��1��min��1
B. 200��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ25
C. �����������200�����µ�100����ԭƽ��һ�����ƻ��������淴Ӧ���ʾ�����
D. ��ͼ�ҿ�֪����ӦxA��g����yB��g��![]() zC��g������H<0����a��2
zC��g������H<0����a��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���Ӧ�У�������ȡ����Ӧ����(����)
A.������ϩ�ֱ�ʹ��ˮ��ɫ
B.������ֱ���NaOH��ˮ��Һ��NaOH�Ĵ���Һ�з�Ӧ
C.��ϩ���ױ�ʹ����KMnO4��Һ��ɫ
D.�����ױ���һ������������ᷴӦ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com