
| A. | 0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.2NA | |
| B. | 1.2gNaHSO4固体中含有的阳离子数目为0.02NA | |
| C. | Na2O2与足量CO2反应生成2.24L O2,转移电子数为0.2NA | |
| D. | 4.6 g NO2和N2O4混合物中含有的原子总数为0.3NA |
分析 A.铁与氯气反应生成氯化亚铁,氯气不足时,应依据氯气的量计算转移电子数;
B.硫酸氢钠中阴离子为硫酸氢根离子;
C.气体状况未知;
D.NO2和N2O4混合物中的N、O比为1:2,n(NO2)为0.1mol,因此含有的原子数为0.3mol.
解答 解:A..1mol Fe在0.1mol Cl2中充分燃烧生成氯化铁,氯气不足,0.1mol Cl2生成0.2molCl-,得到0.2mol电子,转移的电子数为0.2NA,故A正确;
B.硫酸氢钠中阴离子为硫酸氢根离子,1.2gNaHSO4固体的物质的量为0.01mol,含有的阳离子数目为0.01NA,故B错误;
C.气体状况未知,Vm未知,生成氧气的物质的量无法计算,无法计算转移电子数,故C错误;
D.NO2和N2O4混合物中的N、O比为1:2,n(NO2)为0.1mol,因此含有的原子数为0.3mol,原子总数为0.3NA,故D正确;
故选:AD.
点评 本题考查了阿伏伽德罗常数,掌握公式的使用、气体摩尔体积使用条件和对象是解题关键,注意硫酸氢钠的构成,题目难度不大.


科目:高中化学 来源: 题型:解答题
 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +2KMnO4$\stackrel{△}{→}$
+2KMnO4$\stackrel{△}{→}$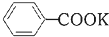 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O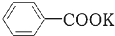 +HCl→
+HCl→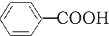 +KCl
+KCl| 名称 | 相对分 子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
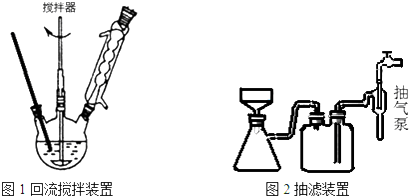
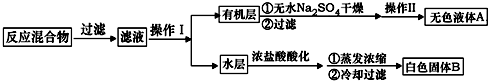
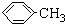 .操作Ⅱ为蒸馏.
.操作Ⅱ为蒸馏.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,则该反应的△H<0 | |
| B. | 检验某物质是否含有Fe2O3的操作步骤是:样品粉碎→加水溶解→过滤,向滤液中滴加KSCN溶液 | |
| C. | 锌与稀硫酸反应时加少量硫酸铜,反应加快的主要原因是Cu2+水解增大了H+浓度 | |
| D. | 甲基苯环上的一个氢原子被含3个碳原子的烷基取代的产物可能有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精、冰醋酸分别属于电解质、弱电解质 | |
| B. | 冶炼金属钠、铁,工业常用的方法分别是电解法、热分解法 | |
| C. | 铝热反应、实验室制氢气都属于置换反应 | |
| D. | 冰醋酸、碱式碳酸铜分别属于:酸、碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
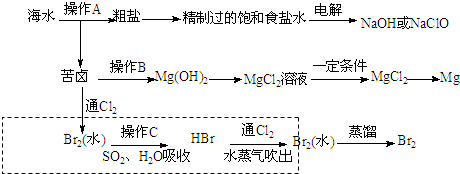
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg变为MgO时化合价升高,因此,Mg在该反应中作还原剂 | |
| B. | KMnO4受热分解时,Mn元素化合价一方面升高一方面降低,因此,在该反应中Mn元 素既被氧化又被还原 | |
| C. | 凡是氧化还原反应都能造福人类 | |
| D. | 在反应2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑中H2O是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
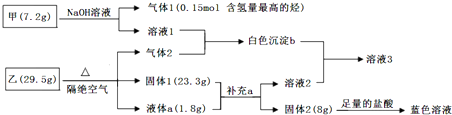
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4L CO中一定含有6.02×1023个分子 | |
| B. | 在标准状况下,22.4L CH4与18g H2O所含有的电子数均为10 NA | |
| C. | 常温常压下,16g O2 与16gO3含有的分子数相同 | |
| D. | 0.1 mol/L K2SO4 溶液中含有 K+为0.2 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com