
下列说法正确的是 ( )
①电解质溶液导电过程属于化学变化
②稀有气体不活泼的原因是它们原子的最外层都达到8电子稳定结构
③FeC12、CuS、NO都不能通过化合反应来制取
④SiO2是制造光导纤维的材料
A.②④ B.①④ C.①③④ D.②③
科目:高中化学 来源: 题型:
1 000 K时反应C(s)+2H2(g)
 CH4(g)的K=8.28×107 (mol·L-1)-1,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述反应( )
CH4(g)的K=8.28×107 (mol·L-1)-1,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述反应( )
A.正向移动 B.逆向移动 C.达到平衡 D.不一定
查看答案和解析>>
科目:高中化学 来源: 题型:
消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________ (填序号)。
A.Cl2 B.H2O2
C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O+H2O2===A+NH3↑,则生成物A的化学式为________,H2O2被称为“绿色氧化剂”的理由是_________________________________________。
(3)漂白剂亚氯酸钠(NaClO2)在常温下、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子数约为________。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是__________________________________(用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应所得溶液中一定只含一种溶质的是 ( )
A.向NaOH溶液中通入CO2 B.向Ca(OH)2溶液中通入Cl2
C.向蒸馏水中加入少量金属Na D.向A12(SO4)3溶液中滴入Ba(OH)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z在周期表中位置如右图。下列说法正确的是 ( )
A.若它们均为金属元素,则X与氧元素组成的物质中一定只含离子键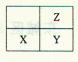
B.若它们的原子最外层电子数之和为11,则它们均为非金属元素
C.它们的原子最外层电子数的大小顺序一定是Z=Y>X
D.Z元素的最高化合价不一定大于X元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是 ( )
A.向含有CaCO3沉淀的水中通入CO2 至沉淀恰好溶解,再向溶液中加入NaHCO3 饱和溶液,又有CaCO3沉淀生成。
B.向Na2 CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2 CO3的物质的量之比为1:2.
C.等质量的NaHCO3和Na2 CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2 CO3饱和溶液中通入CO2,有晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量的主族金属元素的单质A、B、C,分别与足量的稀盐酸反应,同条件下得氢气的体积依次为VA、VB、VC,已知VB=2VC,VA=VB+VC,则在C的生成物中该金属元素的化合价为 ( )
A.+1 B.+2 C.+3 D.+4
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol·L-1Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法正确的是
A.图中A点对应溶液的pH:a=1
B.生成沉淀的最大质量m=2.33g
C.原混合液中c(HCl)=0.2mol·L-1
D.当V[Ba(OH)2(aq)]=30mL时,有关离子浓度大小:
c(Cl-)>c(Ba2+)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.2008年5月12日汶川大地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上制取漂白粉的化学方程式为______________________________________。
(2)漂白粉的有效成分是(填化学式)_______________________________。
(3)漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸。化学反应方程式为________________________________________________________________________
________________________________________________________________________。
Ⅱ.钢铁“发蓝”是在钢铁表面形成一层致密的Fe3O4薄膜的技术。其中一种方法是将钢铁制品浸到NaNO2和浓NaOH的混合溶液中加热到130℃。其过程可以用如下方程式表示:
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②6Na2FeO2+NaNO2+5H2O===3Na2Fe2O4+NH3↑+7NaOH
③Na2FeO2+Na2Fe2O4+2H2O===Fe3O4+4NaOH
则反应②中的氧化剂是________(填化学式),整个过程中,每有168 g Fe参加反应,则转移________ mol 电子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com