
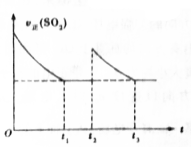
 一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )
一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )| A. | t2时改变的条件是:只加入一定量的SO2 | |
| B. | t1时平衡常数K1大于t3时平衡常数K2 | |
| C. | t1时平衡混合气的$\overline{{M}_{1}}$大于t3时平衡混合气的$\overline{{M}_{2}}$ | |
| D. | t1时平衡混合气中的SO3的体积分数等于t3时平衡混合气中SO3的体积分数 |
分析 A.催化剂改变化学反应速率,但不影响平衡的移动;
B.平衡常数只与温度有关系;
C.据$\overline{M}$=$\frac{m}{n}$进行分析;
D.根据以上分析可知,t1 和t3时,平衡所处的状态一样,则平衡时n(SO3)不变,据此进行分析.
解答 解:A.t2时SO2的正反应速率瞬间变大,然后逐渐降低,最终和要平衡相同,说明平衡只是暂时被破坏,平衡并没有发生移动,改变的条件可以是使用了催化剂,故A错误;
B.平衡常数只与温度有关系,一定温度下,故温度不变,则在t1 时平衡常数K1 等于t3 时平衡常数K2,故B错误;
C.根据以上分析可知,t1 和t3时,平衡所处的状态一样,则n相等,又因为化学反应前后质量守恒,则m相等,则$\overline{M}$=$\frac{m}{n}$相等,故 t1 时平衡混合气的等于t3 时平衡混合气的,故C错误;
D.根据以上分析可知,t1 和t3时,平衡所处的状态一样,则平衡时n(SO3)不变,故t1时平衡混合气中的SO3的体积分数等于t3时平衡混合气中SO3的体积分数,故D正确,
故选D.
点评 本题考查了外界条件对反应速率影响图象分析,注意该图象只体现正反应速率,以及平衡常数是温度的函数,题目难度中等.


科目:高中化学 来源: 题型:选择题

| A. | 锌片为正极 | |
| B. | 该电池工作时电能转化为化学能 | |
| C. | 该电池的总反应为Zn+2H+═Zn2++H2↑ | |
| D. | 电子由铜片通过导线流向锌片 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 I.(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.图中t1 时引起平衡移动的条件可能是增大压强.
I.(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.图中t1 时引起平衡移动的条件可能是增大压强.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
| A. | HCl、BaCl2、AgNO3、Na2CO3 | B. | AgNO3、HCl、BaCl2、Na2CO3 | ||
| C. | BaCl2、Na2CO3、AgNO3、HCl | D. | AgNO3、HCl、Na2CO3、BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
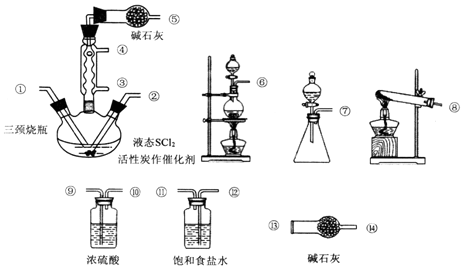
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3 | B. | Fe3O4 | C. | Fe4O5 | D. | Fe6O7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
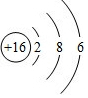 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 泡沫灭火器利用硫酸铝和小苏打溶液反应的产物来灭火 | |
| B. | 为使水果尽快成熟,可用浸泡过高锰酸钾溶液的硅土吸收水果产生的乙烯 | |
| C. | 煤的干馏、燃煤烟气的脱硫、煤的液化和气化等过程都是化学变化 | |
| D. | 面粉生产中禁止添加的过氧化钙(CaO2)阴、阳离子的个数之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用乙醇的还原性以及Cr3+、Cr2O72-的颜色差异来检验是否酒后驾车 | |
| B. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是产生雾霾天气的主要因素 | |
| C. | 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+═Cl2↑+H2O | |
| D. | 天然纤维与合成纤维的主要成分都部是纤维素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com