
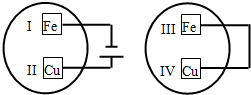 把铁片和铜片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示),经一段时间后,观察到溶液变红的区域是( )
把铁片和铜片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示),经一段时间后,观察到溶液变红的区域是( )| A. | II和III附近 | B. | II和IV附近 | C. | I和III附近 | D. | I和IV附近 |
分析 第一个装置是电解池,与电源正极相连的是电解池的阳极,所以铜为阳极,铁为阴极,溶液中的H+在阴极Ⅰ处得电子,破坏了铁片附近水的电离平衡,使得OH-浓度增大,所以Ⅰ处变红;第二个装置是原电池,活泼金属铁为负极,溶液中的氧气在正极Ⅳ处得电子生成OH-,所以Ⅳ处变红.
解答 解:第一个装置是电解池,与电源正极相连的是电解池的阳极,所以铜为阳极,铁为阴极,溶液中的H+在阴极Ⅰ处得电子,2H++2e-=H2↑,破坏了铁片附近水的电离平衡,使得OH-浓度增大,所以Ⅰ处变红;
第二个装置是原电池,活泼金属铁为负极,铜为正极是Ⅳ,溶液中的氧气在正极Ⅳ处得电子生成OH-,O2+2H2O+4e-=4OH-,所以Ⅳ处变红;
故选D.
点评 本题考查了原电池和电解池的工作原理的应用,主要是电解反应的离子变化.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 干冰汽化需吸收大量的热,这个变化是吸热反应 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 | |
| D. | 放热反应的发生无需任何条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X原子的最外层电子数比Y原子最外层电子数多 | |
| B. | X的最高价氧化物水化物的酸性比Y的最高价氧化物水化物的酸性强 | |
| C. | 与H2化合时X形成的单质比Y形成的单质容易 | |
| D. | X单质可以把Y从其氢化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N4是N2的同素异形体 | |
| B. | 等质量的N4和N2,N4体积是N2体积的一半 | |
| C. | 相同质量的N4和N2所含原子个数比为1:2 | |
| D. | N4的摩尔质量是56g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去Na2CO3固体中少量NaHCO3:加热 | |
| B. | 除去CO2中少量SO2:通过饱和NaHCO3溶液 | |
| C. | 除去氯气中少量氯化氢:通过氢氧化钠溶液 | |
| D. | 除去氧化铁中少量氧化铝:加入过量的烧碱溶液后,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
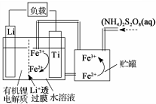
| A. | Li+透过膜除允许Li+通过外,还允许H2O分子通过 | |
| B. | 放电时,进入贮罐的液体发生:S2O32-+2Fe2+=2Fe3++2SO42- | |
| C. | 充电时,钛电极与外电源的正极相连 | |
| D. | 充电时,电池内部发生的总反应为Li++Fe2+=Li+Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 天然气燃烧 | |
| B. | 硫酸与氢氧化钡溶液反应 | |
| C. | 铁与盐酸反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的充分反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com