
| A. | 用电子式表示溴化氢的形成过程为: | |
| B. | 海水中Br-的电子式为: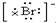 | |
| C. | 海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl | |
| D. | 氯离子的结构示意图为: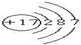 |
分析 A.溴化氢为共价化合物,分子中不存在阴阳离子;
B.溴离子为阴离子,其电子式中需要标出最外层电子;
C.2NaBr+Cl2═Br2+2NaCl为化学方程式,不是离子方程式;
D.氯离子最外层达到8个电子,题中表示的为氯原子.
解答 解:A.溴化氢分子中不存在阴阳离子, ,故A错误;
,故A错误;
B.溴离子最外层达到8个电子稳定结构,电子式需要标出阴离子所带电荷及最外层电子,溴离子的电子式为: ,故B正确;
,故B正确;
C.海水中通入氯气时发生反应的离子方程式为:2Br-+Cl2=Br2+2Cl-,故C错误;
D.氯离子最外层达到8电子稳定结构,氯离子正确的结构示意图为: ,故D错误;
,故D错误;
故选B.
点评 本题考查了电子式、离子方程式、离子结构示意图等化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及正确表示方法,明确离子结构示意图与原子结构示意图的表示方法及区别.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 为放热反应 | |
| B. | 为吸热反应 | |
| C. | 反应过程中热能转化为化学能 | |
| D. | 反应物的总能量低于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH(OH)COOH | B. | HOOC-COOH | ||
| C. | CH3CH2CH2OH | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳可做有机溶剂 | |
| B. | 可用工业酒精勾兑白酒 | |
| C. | 甲烷是清洁高效的燃料 | |
| D. | 用二氯甲烷只有一种结构证明甲烷空间结构是正四面体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 每消耗l mol CH4可以向外电路提供8 mol e- | |
| B. | 负极上CH4失去电子,电极反应式为CH4+10OH--8e-═CO32-+7H2O | |
| C. | 电池放电时,正极附近的pH不断降低 | |
| D. | 电池放电时,溶液中的OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
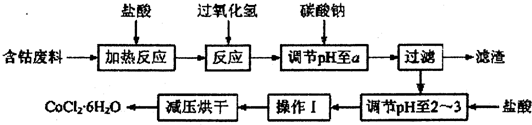
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁在氧气中燃烧生成四氧化三铁 | B. | 常温下,铁在浓硫酸中会发生钝化 | ||
| C. | 铁与盐酸反应生成氯化铁与氢气 | D. | 铁是一种银白色金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com