
| A. | “滴水石穿、绳锯木断”不涉及化学变化 | |
| B. | 明矾净水的原理和“84”消毒液消毒的原理不相同 | |
| C. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| D. | 汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的 |
分析 A.水中溶解的二氧化碳与碳酸钙反应生成碳酸氢钙;
B.明矾净水是利用胶体的吸附性,“84”消毒液消毒是利用物质的强氧化性;
C.雾霾天气的形成与粉尘污染、汽车尾气有关;
D.汽油不完全燃烧生成CO.
解答 解:A.水中溶解的二氧化碳与碳酸钙反应生成碳酸氢钙,所以滴水石穿过程中涉及化学变化,故A错误;
B.明矾水解生成氢氧化铝胶体,胶体具有吸附性而吸附水中的杂质,所以能净水,“84”消毒液中含有次氯酸盐,具有强氧化性,能杀菌消毒,所以明矾净水的原理和“84”消毒液消毒的原理不同,故B正确;
C.氟利昂作制冷剂会导致臭氧空洞,雾霾天气的形成与粉尘污染、汽车尾气有关,故C错误;
D.汽车尾气中含有的氮氧化物是放电条件下氮气与氧气反应生成,汽油不完全燃烧生成CO,故D错误;
故选B.
点评 本题考查了化学变化、净水原理、合成材料、干燥剂,侧重于考查化学知识在生产生活中的应用,题目难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 定量分析--测沸点 | |
| B. | 定性分析--滴入酸性高锰酸钾溶液 | |
| C. | 定量分析--使用银氨溶液 | |
| D. | 定性分析--与新制氢氧化铜悬浊液共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 相关实验 | 预期目的 | |
| A | 向少量燃尽火柴头的浸泡液中滴加稀硫酸,AgNO3 | 验证火柴头含有氯元素 |
| B | 向两支装有等体积,等浓度的H2O2溶液试管中分别加入1mol等浓度的FeCl3溶液、CuSO4溶液 | 催化效果:Fe3+>Cu2+ |
| C | 向待测溶液中加NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝的气体 | 证明原溶液中含有NH4+ |
| D | 向等浓度的NaCl、KI混合液中逐滴加入AgNO3溶液先出现黄色沉淀 | K(sp),AgCl>AgI |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、N2、CO2均属于非电解质 | B. | NO2、CO2、H2O均属于氧化物 | ||
| C. | CH4、NO2、CO2均属于非极性分子 | D. | 该反应属于置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | B. | 碳原子的结构示意图: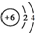 | ||
| C. | CO2分子的结构式: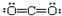 | D. | 聚丙烯的结构简式: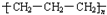 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
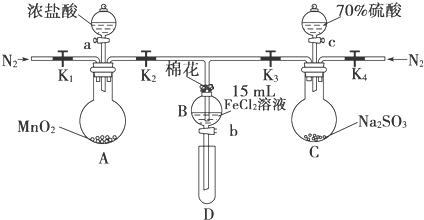
| 过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 是酸性氧化物,能与NaOH溶液反应 | |
| B. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| C. | Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com