
| ���� | ���� | ���� |
| һ | ȡ��ɫ�������ձ��У�������ˮ����ϴ�ӡ����� | ��ɫ����δ�ܽ� |
| �� | ȡ����������ϡ�����н��г���ܽ� | ���������� |
| �� | ��ȡ�����������Һ���Թ�A�У����μ����軯����Һ | ��ҺΪѪ��ɫ |
| �� | ��ȡ�����������Һ���Թ�B�У��μ�����KMnO4��Һ | ����KMnO4��Һ��ɫ |
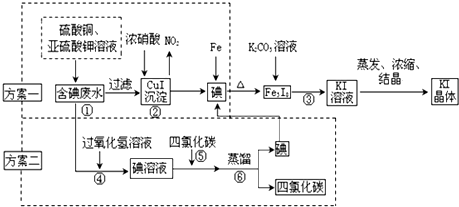
���� ����һ�������ˮ�м�������ͭ�����������Һ������������ԭ��Ӧ����CuI������أ�Ȼ����˵õ�CuI���� CuI�����м���Ũ���ᣬ����������ԭ��Ӧ���ɶ�������������ͭ�͵⣬��ȡ�õ��⣬����м���Fe��������Ӧ����Fe3I8����Fe3I8�м���̼�����Һ����KI����KI��Һ����Ũ����ȴ�ᾧ�õ�KI���壻
�����������ˮ�м������������Һ������������ԭ��Ӧ���ɵ��ˮ�������Һ�м������Ȼ�̼��ȡ������õ�������Ȼ�̼��
I�����������£�CuI��FeCl3����������ԭ��Ӧ�����������ӡ�ͭ���Ӻ͵⣻
������ʱ�õ��IJ���������������������ƿ���ƾ����⣬��ȱ�ٵIJ���������������ƿ�����������¶ȼƣ�
��1�����������£������Ӻ͵�������ӷ���������ԭ��Ӧ���ɵ��ˮ��
��2������5I-+IO3-+6H+=3I2��+3H2O��I2+2S2O32-=2I-+S4O62-�ã�
5I-��3I2��6S2O32-�����ݵ����Ӻ�������������֮��Ĺ�ϵʽ����������������
������1�����������Թ������Һ���ù��˷�����
��2������Ԫ���غ�֪����ɫ�����к���FeԪ�أ��ú�ɫ���ʲ�����ˮ���ܺ��ᷴӦ��û���������ɣ�Ӧ�����ڼ�������������еõ�����Һ����KSCN��Һ����Һ��ΪѪ��ɫ��˵�����������ӣ������еõ�����Һ�������Ը��������Һ�����Ը��������Һ��ɫ��˵�������������ӣ�
��� �⣺����һ�������ˮ�м�������ͭ�����������Һ������������ԭ��Ӧ����CuI������أ�Ȼ����˵õ�CuI���� CuI�����м���Ũ���ᣬ����������ԭ��Ӧ���ɶ�������������ͭ�͵⣬��ȡ�õ��⣬����м���Fe��������Ӧ����Fe3I8����Fe3I8�м���̼�����Һ����KI����KI��Һ����Ũ����ȴ�ᾧ�õ�KI���壻
�����������ˮ�м������������Һ������������ԭ��Ӧ���ɵ��ˮ�������Һ�м������Ȼ�̼��ȡ������õ�������Ȼ�̼��
I�����������£�CuI��FeCl3����������ԭ��Ӧ�����������ӡ�ͭ���Ӻ͵⣬���ӷ���ʽΪ2CuI+4Fe3+�T4Fe2++2Cu2++I2����
�ʴ�Ϊ��2CuI+4Fe3+�T4Fe2++2Cu2++I2����
������ʱ�õ��IJ���������������������ƿ���ƾ����⣬��ȱ�ٵIJ���������������ƿ�����������¶ȼƣ��ʴ�Ϊ��������ƿ�����������¶ȼƣ�
��1�����������£������Ӻ͵�������ӷ���������ԭ��Ӧ���ɵ��ˮ�����ӷ���ʽΪ5I-+IO3-+6H+=3I2��+3H2O��
�ʴ�Ϊ��5I-+IO3-+6H+=3I2��+3H2O��
��2������5I-+IO3-+6H+=3I2��+3H2O��I2+2S2O32-=2I-+S4O62-�ã�
5I-��3I2��6S2O32-��
�����Ƶ�KI��Һ���ʵ���Ũ��Ϊc��
5I-��3I2��6S2O32-��
5 6
0.02cmol 0.3mol/L��0.02L
5��6=0.02cmol����0.3mol/L��0.02L��
c=$\frac{0.3mol/L��0.02L��5}{6��0.02mol}$=0.25
��ˮ�е����������=$\frac{0.25mol/L��0.1L��127g/mol}{1000g}$��100%=0.32%��
�ʴ�Ϊ��0.32%��
������1�����������Թ������Һ���ù��˷������ò��������ǹ��ˣ��ʴ�Ϊ�����ˣ�
��2������Ԫ���غ�֪����ɫ�����к���FeԪ�أ��ú�ɫ���ʲ�����ˮ���ܺ��ᷴӦ��û���������ɣ�Ӧ�����ڼ�������������еõ�����Һ����KSCN��Һ����Һ��ΪѪ��ɫ��˵�����������ӣ������еõ�����Һ�������Ը��������Һ�����Ը��������Һ��ɫ��˵��������������
�ٸ������Ϊ��ɫ��Һ����������ɫ������Ҫ���ָʾ����
�ʴ�Ϊ����KMnO4��Һ��������ָʾ����
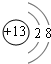
��ͨ�����Ϸ���֪���ú�ɫ�����к���Fe��OԪ���Һ���+2�ۡ�+3��FeԪ�أ�����ΪFe3O4���ʴ�Ϊ��Fe3O4��
���� ���⿼�����ʷ�����ᴿ��Ϊ��Ƶ���㣬�漰���ʳɷ��жϡ���ѧ����ʽ�ļ��㡢������ԭ��Ӧ�����ʷ�����ᴿ������ѡȡ������ѡȡ��֪ʶ�㣬���ؿ���ѧ�������жϼ�ʵ�������������ȷ�������ʼ����ʷ����ᴿ�����ǽⱾ��ؼ���֪���������ӡ������Ӽ��鷽������Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
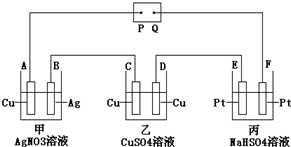
| A�� | P�ǵ�Դ������ | |
| B�� | F���Ϸ����ķ�ӦΪ��4OH--4e-=2H2O+O2�� | |
| C�� | ���ʱ���ס��ҡ��������У���E��F�����⣬����缫���μ��˷�Ӧ | |
| D�� | ͨ��׳���Һ��pH��С���ҳ���Һ��Ũ����������Һ��pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.5mol����Fe����������������ȫȼ�գ�ʧȥ4NA������ | |
| B�� | ��25g��������Ϊ60%������ˮ��Һ�У�������ԭ����ΪNA | |
| C�� | 7.8��gNa2S��Na2O2���Ļ�����У����е�������������0.15NA | |
| D�� | ��5��107Pa��500��C������ý�����£�1molN2��3molH2�����ɰ���������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Na2O2+2H2O�T4NaOH+O2�� | B�� | Mg3Cl2+2NaOH�TMg��OH��2��+2NaCl | ||
| C�� | 2NaOH+Cl2�TNaOCl+H2O | D�� | NH4Cl+NaO�TNaCl+NH3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S��g��+O2��g��=SO2��g���ų���������297.23kJ | |
| B�� | S��g��+O2��g��=SO2��g���ų�����С��297.23kJ | |
| C�� | ��H=-297.23kJ•mol-1��ʾ����S��ȼ���� | |
| D�� | �γ�1molSO2��ѧ���ͷŵ����������ڶ���1molS��s����1molO2��g����ѧ�����յ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
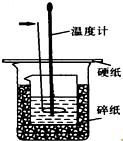 50ml0.50mol•L-1������50mL0.55mol•L-1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȣ��ش��������⣺
50ml0.50mol•L-1������50mL0.55mol•L-1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3CH2OH | B�� | COOH-CHOH-CHCl-COOH | ||
| C�� | CFCl3 | D�� | CH2OH-CHOH-CH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
��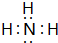 ��G�ĽṹʽΪ
��G�ĽṹʽΪ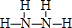 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com