
科目:高中化学 来源: 题型:
在2L恒容密闭容器中投入足量M(s)和一定量的R(g),发生反应为
M(s)+R(g) X(g)+Y(g)
X(g)+Y(g)  ;所得实验数据如下表所示:
;所得实验数据如下表所示:
| 实验 | 温度/℃ | 起始时R的物质的量/mol | 平衡时气体总物质的量/mol |
| ① | 300 | 2.00 | 2.80 |
| ② | 400 | 2.00 | 3.00 |
| ③ | 400 | 4.00 | a |
下列推断正确的是
A.上述反应中, <0
<0
B.实验②中,该反应的平衡常数K=0.5
C.实验①经4 min达到平衡,0~4 min内υ(X)=0.2mol•L1•min1
D.实验③中a=6.00
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述的实验能达到预期目的的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 滴定实验中,用待测液润洗锥形瓶2~3次 | 避免造成实验误差 |
| B | 向氯水中滴加AgNO3、稀HNO3溶液,产生白色沉淀 | 验证氯水中含有Cl- |
| C | 向盛有沸水的烧杯中滴加饱和氯化铁溶液并长时间煮沸 | 制备氢氧化铁胶体 |
| D | 向2 mL 1 mol·L-1 NaOH溶液中先加入3滴1 mol·L-1 MgCl2溶液,再加入3滴1 mol·L-1 FeCl3溶液 | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列化合物:
①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O,回答下列问题。
(1)NH4Cl溶液显________性,用离子方程式表示原因________,其溶液中离子浓度大小顺序为________。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=________,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=________。
(3)已知纯水中存在如下平衡:H2O+H2OH3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是________(填字母序号)。
A.向水中加入NaHSO4固体
B.向水中加Na2CO3固体
C.加热至100 ℃[其中c(H+)=1×10-6 mol·L-1]
D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH溶液和⑦NH3·H2O溶液分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等 ,则m________(填“<”、“>”或“=”)n。
,则m________(填“<”、“>”或“=”)n。
(5)除⑧H2O外,若其余7种物质的溶液的物质的量浓度相同,则这7种物质的溶液按pH由大到小的顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列颜色不属于因化学反应而产生的现象的是
A.无色试剂瓶中的浓硝酸呈黄色
B.久置的KI溶液呈黄色
C.新制氯水久置后变为无色
D.在普通玻璃导管口点燃纯净氢气时,火焰呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
关于某溶液所含离子检验的方法和结论正确的是
A.加入BaCl2溶液有白色沉淀生成,加稀盐酸沉淀不消失,原溶液一定有SO42
B.加入AgNO3溶液有白色沉淀生成,加稀盐酸沉淀不消失,原溶液一定有Cl-
C.加入盐酸产生能使澄清石灰水变浑浊的气体,原溶液中可能有CO32-或SO32-
D.加入NaOH并加热,产生使湿润蓝色石蕊试纸变红的气体,原溶液是铵盐溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
把含硫酸铵和硝酸铵的混合液2a L分成两等份。一份加入bmol NaOH并加热,恰好把NH3全部赶出;另一份需消耗cmol BaCl2沉淀反应恰好完全,则原溶液中NO3- 的浓度为 ( )
A  B
B 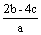 C
C  D
D 
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述中正确的是( )
A.CS2为Ⅴ形的极性分子
B.ClO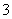 的空间构型为平面三角形
的空间构型为平面三角形
C.SF6中S原子为sp6杂化
D.SiF4和SO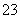 的中心原子均为sp3杂化
的中心原子均为sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
钠、铝、铁是三种重要的金属。请回答:
(1)将一小块金属钠投入水中,可观察到的实验现象是_____________(填字母)。
a.钠浮在水面上 b.钠熔成小球 c.小球四处游动 d.溶液变红
(2)铝与氢氧化钠浓溶液反应的化学方程式为_______________________________。
(3)三种金属中,常温下遇浓硫酸或浓硝酸不会发生钝化现象的是 (填化学式)。
(4)三种金属在一定条件下均能与水发生反应。其中铁与水蒸气在高温下反应的化学方程式为 。三种金属中,能与冷水发生剧烈反应的是 ,由此说明,钠的金属性比铁和铝 (填“强”或“弱”)。
(5)将烧得红热的铁丝伸到盛有氯气的集气瓶中,可观察到 。该反应的化学方程式为__________________________________________。
(6)某些补铁剂成分中含有硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是 (填序号)。
①稀盐酸 ②石蕊溶液 ③KSCN溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com