
| A. | 氧化还原反应的本质是化合价生了变化 | |
| B. | 化合价升高的物质被氧化 | |
| C. | 得到电子的物质被氧化 | |
| D. | 氧化还原反应中,先有氧化后有还原 |
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 澄清石灰水与碳酸氢钠溶液 | B. | 澄清石灰水与碳酸氢铵溶液 | ||
| C. | 氢氧化钠溶液与碳酸氢钙溶液 | D. | 澄清石灰水与碳酸氢钙溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28.1 | B. | 30.2 | C. | 33.1 | D. | 34.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大C的浓度 | B. | 增大压强 | C. | 升高温度 | D. | 加催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
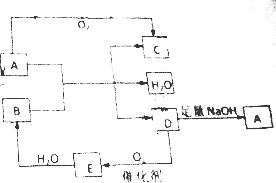 A、B、C、D、E五种物质都含有同一种元素,其中D在常温下为无色有刺激性气味的有毒气体,在一定条件下有如图所示的转化关系.
A、B、C、D、E五种物质都含有同一种元素,其中D在常温下为无色有刺激性气味的有毒气体,在一定条件下有如图所示的转化关系. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HA溶液中由水电离出来的c(H+)=10-13mol/L | |
| B. | 加入NaOH溶液过程中,$\frac{c({H}^{+})}{c(HA)}$比值减小 | |
| C. | 混合液中:c(Na+)=c(A-)+c(HA) | |
| D. | 混合液中HA电离常数Ka增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com