
| A. | 常温常压下,16g O3所含的氧原子数目为NA | |
| B. | 标准状况下,O2的体积取决于O2分子间的距离 | |
| C. | 摩尔是用来衡量微观粒子多少的一种物理量 | |
| D. | 若气体摩尔体积为22.4 L/mol,则所处条件为标准状况 |
分析 A.依据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算解答;
B.分依据PV=nRT,结合分子间平均距离受温度、压强影响;
C.摩尔是物质的量单位;
D.气体摩尔体积与温度和压强有关,气体摩尔体积为22.4L•mol-1,未必所处条件为标准状况.
解答 解:A.臭氧是由氧原子构成,常温常压下,16g O3所含的氧原子数目为$\frac{16g}{16g/mol}$×NA=NA,故A正确;
B.分依据PV=nRT,标况下O2的体积取决于O2分子数目,标况下距离是定值,故B错误;
C.物质的量是用来衡量微观粒子多少的一种物理量,故C错误;
D.气体摩尔体积是单位物质的量的气体所占有的体积,气体体积与温度和压强有关,温度升高,气体体积增大,压强增大,气体体积减小,所以不是在标况下,气体摩尔体积有可能为22.4 L•mol-1,故D错误;
故选:A.
点评 本题主要考查的是摩尔的定义以及气体摩尔体积的定义,属于概念性理解题,注意影响气体体积的因素有物质的量、温度和压强,注意总结,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | N2为$\frac{1}{3}$mol•L-1 | B. | NH3为$\frac{10}{3}$mol•L-1 | ||
| C. | H2为5.5mol•L-1 | D. | N2为1.5mol•L-1,H2为3.5mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64gCaC2中含有的共价键数目为3NA | |
| B. | 20gD2O与20gH218O含有的中子数均为11NA | |
| C. | 4.6gNO2在标准状况下,含有的分子数为0.1 NA | |
| D. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加催化剂 | B. | 扩大容器体积 | C. | 升高温度 | D. | 增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I- | |
| B. | NaHCO3溶液中:Na+、K+、SO42-、AlO2- | |
| C. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、SiO32-、NO3- | |
| D. | 水电离出的c(H+)=1×10-13mol/L的溶液:Na+、K+、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  观察Fe(OH)2的生成 | |
| B. | 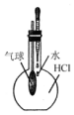 用图所示方法验证HCl气体易溶于水 | |
| C. | 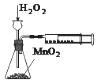 用图定量测定H2O2的分解速率 | |
| D. | 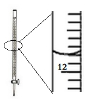 记录滴定终点读数为12.20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极的电极反应式为 Li-e-=Li+ | |
| B. | 正极的电极反应式为2SOCl2+4e-=SO2+S+4Cl- | |
| C. | 若电解液中含有水,则该电池的效率将大大降低 | |
| D. | 若负极有14gLi参加反应,则理论上流过电路中的电子书约为1.204×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,46gNO2与N2O4的混合气体中含有的原子数为3NA | |
| B. | 15.6g Na2O2与过量CO2反应时,转移的电子数为0.4NA | |
| C. | 常温常压下,11.2L二氧化硫中所含的氧原子数等于NA | |
| D. | 1L1mol•L-1的Na2CO3溶液中含有NA个CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com