
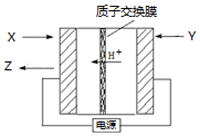
 氨是生产氮肥、尿素等物质的重要原料.电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )
氨是生产氮肥、尿素等物质的重要原料.电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )| A. | Y参与的电极反应为H2+2e-=2H+ | |
| B. | 反应过程中左边区域溶液pH逐渐升高 | |
| C. | 图中所示物质中,X为H2,Y为N2 | |
| D. | 当有3g H+通过质子交换膜时,Z的体积为22.4L |
分析 根据氢离子移动方向可知,X端为阴极,Y端为阳极,则通入H2的一极为化合价升高,发生氧化反应,该极为阳极Y端;合成氨的阴极X端上氮气得到电子生成氨气,据此分析解答.
解答 解:A、Y端为阳极,H2失电子发生氧化反应,电极反应为H2-2e-=2H+,故A错误;
B、反应过程中左边X端为阴极,氮气得到电子结合氢离子生成氨气,所以pH逐渐升高,故B正确;
C、根据氢离子移动方向可知,X端为阴极,Y端为阳极,所以X为N2,Y为H2,故C错误;
D、当有3g即3molH+通过质子交换膜时,则生成1mol氨气即Z的体积在标况下为22.4L,而状况不知,故D错误;
故选B.
点评 本题考查学生电解池的工作原理,难度中等,掌握电极反应是解题关键.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:解答题
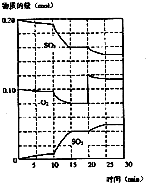 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| B. | 增大压强,正逆反应的化学反应速率都减小 | |
| C. | 升高温度,正反应化学反应速率增大,逆反应化学反应速率减 | |
| D. | 对该反应来说,无沦反应进行到何时,混合气体的总物质的量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15 mol•L-1 | B. | 0.10 mol•L-1 | C. | 0.25 mol•L-1 | D. | 0.40 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 | |
| B. | 电池的正极反应式为:O2+2H2O+4e-═4OH- | |
| C. | 电解后电池中c(KOH)不变;c(Na2CO3)不变 | |
| D. | 电解后电解池中溶液pH变大,且溶液中有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 打开汽水瓶盖时有大量气泡冒出,可用勒夏特列原理解释 | |
| B. | 用铁质自来水管与铜质水龙头连接使用时,连接处的铁水管锈蚀更快 | |
| C. | 锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去 | |
| D. | 海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com