
【题目】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:
Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH1=+489.0 kJ·mol-1,
C(s) +CO2(g)=2CO(g) ΔH2=+172.5kJ·mol-1
则CO(g)还原Fe2O3(s)的热化学方程式为____。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:_____。
(3)将CO2和H2充入1L的密闭容器中,在两种温度下发生反应:
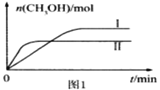
CO2(g) +3H2(g)![]() CH3OH(g) +H2O(g)测得CH3OH的物质的量随时间的变化见图1。
CH3OH(g) +H2O(g)测得CH3OH的物质的量随时间的变化见图1。
①该反应的平衡常数表达式为K=___。
②曲线I、Ⅱ对应的平衡常数大小关系为KⅠ___KⅡ(填“>”或“=”或“<”)。
③一定温度下,往该容器中投入1 molCO2、3 mol H2 ,一段时间后达到平衡。若平衡后气体的压强为开始的0.8倍,则CO2的平衡转化率=____。
【答案】Fe2O3(s)+ 3CO(g)=2Fe(s)+ 3CO2(g) △H=-28.5kJ·mol-1 CO+4OH--2e-=CO32-+2H2O ![]() > 40%
> 40%
【解析】
(1)依据热化学方程式和盖斯定律分析解答;
(2)CO-O2燃料电池(以KOH溶液为电解液),燃料CO在负极失电子发生氧化反应;
(3)①根据平衡常数的概念书写表达式;②根据图像可知,线Ⅱ的反应速率大于线Ⅰ,所以线Ⅱ对应的温度高于线Ⅰ,结合温度对化学平衡常数的影响分析判断;③根据三段式计算解答。
(1)①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJmol-1,②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJmol-1,由盖斯定律①-②×3得到Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5kJmol-1,故答案为:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5kJmol-1;
(2)CO-O2燃料电池(以KOH溶液为电解液),一氧化碳在负极失电子发生氧化反应生成二氧化碳,在氢氧化钾溶液中生成碳酸钾,负极的电极反应式为:CO+4OH--2e-=CO32-+2H2O,故答案为:CO+4OH--2e-=CO32-+2H2O;
(3)①CO2(g) +3H2(g)![]() CH3OH(g) +H2O(g) 的平衡常数表达式为K=
CH3OH(g) +H2O(g) 的平衡常数表达式为K=![]() ,故答案为:
,故答案为:![]() ;
;
②根据图像可知,线Ⅱ的反应速率大于线Ⅰ,所以线Ⅱ对应的温度高于线Ⅰ,而线Ⅱ对应的甲醇的物质的量小,即升高温度,平衡逆向移动,平衡常数变小,即KⅠ>KⅡ,故答案为:>;
③设反应的二氧化碳的物质的量为x,
CO2(g)+3H2(g)CH3OH(g)+H2O(g)
初始(mol): 1 3 0 0
反应(mol): x 3x x x
平衡(mol):1-x 3-3x x x
平衡后气体的压强为开始时的0.8倍,同温同体积时,气体的压强之比等于物质的量之比,因此![]() =0.8,解得x=0.4mol,则CO2的平衡转化率=
=0.8,解得x=0.4mol,则CO2的平衡转化率=![]() ×100%=40%,故答案为:40%。
×100%=40%,故答案为:40%。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金(含铁)空心球为吸收剂的太阳能吸热涂层,铁、镍基态原子未成对电子数各为_____________、________________。
(2)C60可用作储氢材料,已知金刚石中的C-C键的键长为0.154 nm,C60中C-C键键长为0.140~0.145 nm,有同学据此认为C60的熔点高于金刚石,你认为是否正确?_________,阐述理由:________________________________________________________________________。C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有_____个。
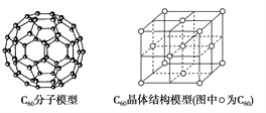
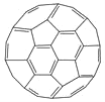
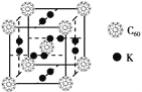
(3)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如下图所示,分子中碳原子轨道的杂化类型为_________;1 mol C60分子中σ键的数目为________。科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为________。
(4)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是______________。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为______个。
(5)请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量: N60>C60>Si60,其原因是:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 以酚酞为指示剂,用盐酸标准液滴定氢氧化钠溶液 | 溶液由红色变为浅红色便立刻读数 | 测得氢氧化钠溶液的浓度偏大 |
B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体 | 有白色沉淀生成,溶液红色变浅 | 证明纯碱溶液呈碱性是由CO32-水解引起的 |
C | 室温下分别测定NaClO溶液、CH3COONa溶液的pH | 前者大 | 酸性:HClO>CH3COOH |
D | NaHCO3溶液中滴入酚酞 | 溶液变红 | 弱酸的酸式盐溶液均呈碱性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告提出了“积极参与全球环境治理,落实减排承诺”。其中氮的化合物的处理和利用是环境科学研究的热点。
(1)氮氧化物与悬浮大气中的海盐粒子相互作用会生成NOCl,涉及的相关反应有:
热化学方程式 | 平衡常数 | |
|
|
|
|
|
|
|
|
|
![]() 、
、![]() 、
、![]() 之间的关系为
之间的关系为![]() ______;
______;![]() 、
、![]() 、
、![]() 的关系为
的关系为![]() ______。
______。
(2)对汽车加装尾气净化装置,可使汽车尾气中含有的CO、![]() 等有毒气体转化为无毒气体:
等有毒气体转化为无毒气体:![]() 对于该反应,温度不同
对于该反应,温度不同![]() ,其他条件相同时,下列图象正确的是______
,其他条件相同时,下列图象正确的是______![]() 填序号
填序号![]() 。
。

(3)用活性炭还原法也可以处理氮氧化物。向某密闭容器中加入一定量的活性炭和NO,发生反应:![]() 在
在![]() 时,反应进行到不同时间测得各物质的浓度如下:
时,反应进行到不同时间测得各物质的浓度如下:
时间 浓度 | 0 | 10 | 20 | 30 | 40 | 50 |
NO |
|
|
|
|
|
|
| 0 |
|
|
|
|
|
| 0 |
|
|
|
|
|
![]() 时,该反应在
时,该反应在![]() 的平均反应速率
的平均反应速率![]() ______;该反应的平衡常数
______;该反应的平衡常数![]() ______;
______;
![]() 后只改变某一条件,根据上表数据判断改变的条件可能是______
后只改变某一条件,根据上表数据判断改变的条件可能是______![]() 填序号
填序号![]() ;
;
A.加入一定量的活性炭 ![]() 恒温恒压充入氩气
恒温恒压充入氩气
C.适当缩小容器的体积 ![]() 加入合适的催化剂
加入合适的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.硫酸氢钠与少量氢氧化钡反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓
C.钠与水反应:Na+2H2O=Na++2OH-+H2↑
D.浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+![]() Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

请回答:
(1)该同学用镊子夹取湿润的红色石蕊试纸靠近试管口,可观察到试纸变蓝,该现象说明氨气溶于水,溶液呈___性。
(2)收集氨气时,请你选择氨气的进气口___(“a”或“b”)。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是___。
(4)以下装置(盛放的液体均为水)可用于吸收多余氨气的是___(填序号)。
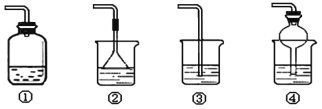
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小时候很想知道天天喝的水究竟由啥构成?到了初中又想查查这瓶纯净水(蒸馏水,体积360mL,密度1g/cm3)中有多少个水分子呢?学了“物质的量”这个能在宏观物质和微观粒子之间架起“桥梁”的物理量,实现这个愿望太简单了。请填空:
这瓶纯净水的质量为______ g,含有水分子______个,含有原子总数_____NA个(NA表示阿伏伽德罗常数),若把这些水变成水蒸气再换算到标准状况下的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。请回答下列问题:
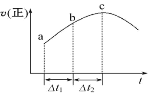
①a~c段反应速率增大的原因是____________。
②有关该反应的说法正确的是________(填字母)。
a.若容器内温度保持不变,可以说明反应达到了平衡状态
b.反应物浓度:a点小于b点
c.反应在c点达到平衡状态
d.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段
e.若容器内气体的平均摩尔质量保持不变,可以说明反应达到了平衡状态
(2)利用反应6NO2+8NH3=7N2+12H2O构成电池的装置如图所示。此装置既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能。请回答下列问题:
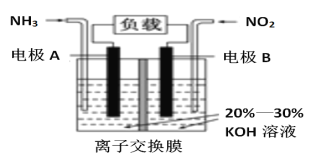
①B电极为______(填“正”或“负”)。
②当有4.48 L NH3(标准状况)参加反应时,转移电子数为________。
③电极A极反应式为______。
④为使电池持续放电,离子交换膜最好选用__________(填“阴”或“阳”)离子交换膜。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应
H2S(g)+3/2 O2(g)=SO2(g)+H2O(g) △H1
2H2S(g)+SO2(g)=3/2 S2(g)+2H2O(g) △H2
H2S(g)+1/2O2(g)=S(g)+H2O(g) △H3
2S(g)=S2(g) △H4
则△H4正确表达式为( )
A. △H4=2/3(△H1+△H2-3△H3) B. △H4=2/3(3△H3-△H1-△H2)
C. △H4=3/2(△H1+△H2+3△H3) D. △H4=3/2(△H1-△H2-3△H3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com