
未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机。这类材料中研究得较多的是化合物G。
(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y。G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体。请推断:①化合物G的化学式为__________________。②由1 mol NH3和0.75 mol E恰好完全反应,化合物E的分子式为_______________________。
(2)粉末状G能够与空气中的氧气和水作用,所得产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料。与氧反应所得的产物还有一种单质;与水反应生成另一种产物是该种单质元素的氢化物。请写出化合物G与水反应的化学方程式_______________________________________________________________________________。
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-xAlxOxY8-x。在接近于1 700 ℃时x的极限值约为4.0,在1 400 ℃时x为2.0,以保持整个化合物呈电中性。试问:①赛伦中各元素的化合价为Si_________,Al_________,O_________,Y_________。赛伦的晶体类型为_________。
科目:高中化学 来源: 题型:阅读理解
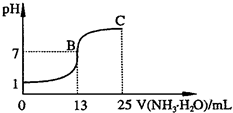 (2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.
(2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y。G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体。请推断:①化合物G的化学式为__________________。②由1 mol NH3和0.75 mol E恰好完全反应,化合物E的分子式为_______________________。
(2)粉末状G能够与空气中的氧气和水作用,所得产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料。与氧反应所得的产物还有一种单质;与水反应生成另一种产物是该种单质元素的氢化物。请写出化合物G与水反应的化学方程式_____________________________________________________________________。
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-xAlxOxY8-x。在接近于1 700 ℃时x的极限值约为4.0,在1 400 ℃时x为2.0,以保持整个化合物呈电中性。试问:①赛伦中各元素的化合价为Si_________,Al_________,O_________,Y_________。赛伦的晶体类型为_________。
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com