
| A. | ①②③⑥ | B. | ③④⑤⑥ | C. | ①②③④⑤ | D. | 全部 |
分析 ①用气态燃料代替液态和固态燃料作为发动机动力来源,可减少污染,提高环境质量;
②含汞电池中会造成土壤和水体的污染;
③减少使用餐巾纸,能节约资源;
④根据分类回收的好进行分析判断;
⑤开发无磷洗涤剂,能防止水体污染;
⑥废弃塑料会造成白色污染进行分析判断.
解答 解:①用气态燃料代替液态和固态燃料作为发动机动力来源,可减少二氧化硫等有害气体的排放,提高环境质量,故①正确;
②含汞电池中会造成土壤和水体的污染,开发生产无汞电池可保护环境,故②正确;
③生成餐巾要消耗大量森林资源,所以减少使用餐巾纸,能节约资源,故③正确;
④分类回收垃圾可变废为宝,最大程度上节约资源,所以分类回收垃圾,故④正确;
⑤含大量磷元素的污水能引起水体富营养化,所以开发无磷洗涤剂,能防止水体污染,故⑤正确;
⑥使用一次性发泡塑料餐具和塑料袋,不仅会造成环境污染,还增加了资源和能源消耗,故⑥错误;
故选C.
点评 本题考查常见环境污染及治理,侧重于化学与生活、生产的考查,有利于培养学生的良好科学素养,树立保护环境的意识,题目难度不大.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{2}{3}$ | B. | $\frac{1}{2}$ | C. | $\frac{1}{3}$ | D. | $\frac{1}{4}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
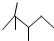 ,有机物 B 与等物质的量的 H2发生加成反应可得到有机物 A.则:
,有机物 B 与等物质的量的 H2发生加成反应可得到有机物 A.则:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
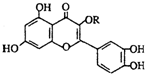 唐山市的市树是国槐,天然维生素P(结构如图)存在于国槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )
唐山市的市树是国槐,天然维生素P(结构如图)存在于国槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )| A. | 若R为甲基则该物质的分子式可以表示为C16H10O7 | |
| B. | 分子中有三个苯环 | |
| C. | lmol该化合物与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol | |
| D. | lmol该化合物最多可与2molBr2完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中SO2、O2、SO3共存 | |
| B. | SO2与SO3的浓度相等 | |
| C. | 容器中SO2、O2、SO3的物质的量之比为2:1:2 | |
| D. | 反应容器中压强不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
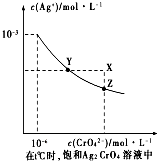 盐在化学工业中有重要的应用,请回答下列问题
盐在化学工业中有重要的应用,请回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:解答题
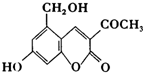 “亮菌甲素”的结构简式为如图所示,它配以辅料丙二1,3,5醇溶成针剂用于临床,而假药“亮菌甲素”是用廉价的二甘醇作为辅料.二甘醇为工业溶剂,有很强的毒性,会使肾功能衰竭.请回答下列问题:
“亮菌甲素”的结构简式为如图所示,它配以辅料丙二1,3,5醇溶成针剂用于临床,而假药“亮菌甲素”是用廉价的二甘醇作为辅料.二甘醇为工业溶剂,有很强的毒性,会使肾功能衰竭.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com