
将1 mol冰醋酸加入到一定量的蒸馏水中最终得到1 L溶液。下列各项中,表明已达到电离平衡状态的是
A.醋酸的浓度达到1 mol·L-1
B.H+的浓度达到0.5 mol·L-1
C.醋酸分子的浓度、醋酸根离子的浓度、H+的浓度均为0.5 mol·L-1
D.醋酸分子电离成离子的速率和离子重新结合成醋酸分子的速率相等
科目:高中化学 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:填空题
I.化工工业中常用乙苯脱氢的方法制备苯乙烯。
已知某温度下:
反应①:CO2 (g) +H2 (g)→CO(g) + H2O(g),ΔH = +41.2 kJ/mol;
反应②: 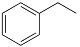 (g)→
(g)→ (g)+H2(g),ΔH= +117.6 kJ/mol;
(g)+H2(g),ΔH= +117.6 kJ/mol;
①②的化学反应平衡常数分别为K1、K2,
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式 ,该反应的化学平衡常数K= (用K1、K2表示)
(2)对于反应①,恒温恒容条件下,向密闭容器中加入2molCO2 和2molH2,当反应达到平衡后,以下说法正确的是
A.因为该反应是吸热反应,所以升高温度,正反应速率增大,逆反应速率减小;
B.若再加入1molCO2、1mol H2,平衡不移动;
C.若再加入CO2则平衡向正反应方向移动,CO的体积分数减小;
D.若充入He,平衡不移动,反应物和产物的浓度都不变;
(3)恒温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2;请在下图中画出t1之后的正逆反应曲线,并作出标注。

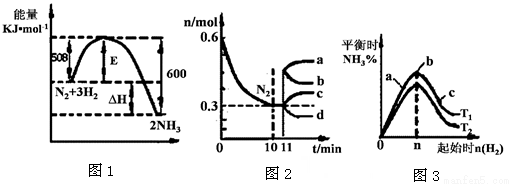
II.一定的条件下,合成氨反应为:N2(g)+3H2(g)  2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
(4)升高温度,该反应的平衡常数 (填“增大”或“减小”或“不变”)。
(5)由图2信息,计算10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)
(6)图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
查看答案和解析>>
科目:高中化学 来源:2016届上海市十三校高三上学期第一次联考化学试卷(解析版) 题型:选择题
下列关于二氧化硅晶体的描述错误的是
A.分子式为SiO2 B.熔化时共价键断裂
C.属于酸性氧化物 D.1mol SiO2中含有4 mol Si-O键
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.向碘化亚铁溶液中通入足量的氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
B.碳酸氢钠溶液与过量的澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
C.用浓盐酸配制的高锰酸钾溶液与过氧化氢反应:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O
D.硫酸氢钠溶液与氢氧化钡溶液以等物质的量混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建晨曦、冷曦、正曦、岐滨四校高二上联考化学卷(解析版) 题型:填空题
某温度下水的离子积为KW =1×10-13,若将此温度下pH=11的NaOH溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),试通过填写以下不同情况时两种溶液的体积比:
(1)若所得混合液为中性,则a∶b= ;
(2)若所得混合液的pH=2,则a∶b= ;
(3)若所得混合液的pH=10,则a∶b= 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
在固定容积的密闭容器中,可逆反应2X(?)+Y(g) Z(s)已达到平衡,此时升高温度则气体的密度增大。下列叙述正确的是( )
Z(s)已达到平衡,此时升高温度则气体的密度增大。下列叙述正确的是( )
A.正反应为放热反应,X可能是气态、液态或固态
B.正反应为放热反应,X一定为气态
C.若X为非气态,则正反应为吸热反应
D.若加入少量的Z,该平衡向左移动
查看答案和解析>>
科目:高中化学 来源:2016届安徽省庐江县六校高三上学期第四次联考化学试卷(解析版) 题型:选择题
常温下,下列各组粒子在指定溶液中能量共存的是( )
A.在酸性KMnO4溶液中:Na+、C2H5OH、NH4+、Cl﹣
B.能溶解CaCO3的溶液中:Fe2+、Ca2÷、Cl﹣、NO3﹣
C.澄清透明的溶液中:Cu2+、Fe3+、SO42﹣、Cl﹣
D.能使淀粉﹣KIO3试纸显蓝色的溶液中:K+、H+、SO42﹣、I﹣
查看答案和解析>>
科目:高中化学 来源:2016届湖南省、修水一中高三上学期联考化学试卷(解析版) 题型:填空题
工业上用某矿渣(主要成分是Cu2O,少量杂质是Al2O3、Fe2O3和SiO2)提取铜的操作流程如下:
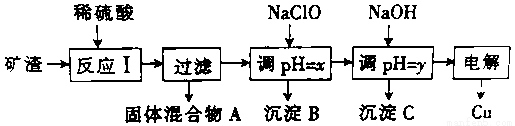
已知:Cu2O+2H+==Cu+Cu2++H2O
沉淀物 |
|
|
|
|
开始沉淀pH | 5.4 | 4.0 | 2.2 | 5.8 |
沉淀完成pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是 (填化学式)。
(2)反应I完成后,铁元素的存在形式为 (填离子符号)。
(3)y的数值范围是 。
(4)若电解法获得Cu 64.0g,则原矿渣中Cu2O的质量是 。
a、144.0g b、大于144.0g c、小于144.0g
(5)下列关于用NaClO调节溶液pH的说法正确的是 。
a、加入NaClO可使溶液的pH降低
b、NaClO能调节pH的主要原因是由于发生反应: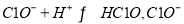 消耗H+,从而达到调节pH的目的
消耗H+,从而达到调节pH的目的
c、NaClO能调节pH的主要原因是由于NaClO水【解析】 OH—消耗H+,从而达到调节pH的目的。
OH—消耗H+,从而达到调节pH的目的。
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列氧化还原反应中,水作为还原剂的是( )
A.Cl2+H2O HCl+HClO B.Br2+SO2+2H2O=H2SO4+2HBr
HCl+HClO B.Br2+SO2+2H2O=H2SO4+2HBr
C.2F2+2H2O=4HF+O2 D.CaO+H2O= Ca(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com