
【题目】已知A是一种装饰品的主要成分,是地壳中含量最高的两种元素形成的化合物。根据下图转化关系,回答下列问题。

(1)A的用途:________(任写一种),B是________,D是________。
(2)写出下列反应的化学方程式:①______________。
(3)写出下列反应的离子方程式:②____________,③_______,⑤____________。
【答案】制光导纤维 Na2SiO3 H2SiO3 Na2CO3+SiO2 ![]() Na2SiO3+CO2↑ CO2+H2O+SiO32—=CO32—+H2SiO3↓(或2CO2+2H2O+SiO32—=2HCO3—+H2SiO3↓) SiO2+2OH-=SiO32—+H2O SiO32—+2H+=H2SiO3↓
Na2SiO3+CO2↑ CO2+H2O+SiO32—=CO32—+H2SiO3↓(或2CO2+2H2O+SiO32—=2HCO3—+H2SiO3↓) SiO2+2OH-=SiO32—+H2O SiO32—+2H+=H2SiO3↓
【解析】
由A是一种装饰品的主要成分,是地壳中含量最高的两种元素形成的化合物可知A是二氧化硅;高温下,二氧化硅与纯碱反应生成硅酸钠和二氧化碳,硅酸钠溶于水与二氧化碳反应生成硅酸沉淀,则D是硅酸;二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,则B是硅酸钠,C是二氧化碳;硅酸钠溶液与盐酸反应生成硅酸沉淀。
(1)A是二氧化硅,二氧化硅是光导纤维的主要成分,是制普通玻璃的原料,B是硅酸钠,D是硅酸,故答案为:制光导纤维;Na2SiO3;H2SiO3;
(2)反应①是高温下,二氧化硅与纯碱反应生成硅酸钠和二氧化碳,反应的化学方程式为Na2CO3+SiO2 ![]() Na2SiO3+CO2↑,故答案为:Na2CO3+SiO2
Na2SiO3+CO2↑,故答案为:Na2CO3+SiO2 ![]() Na2SiO3+CO2↑;
Na2SiO3+CO2↑;
(3)反应②是硅酸钠溶于水与二氧化碳反应生成硅酸沉淀和碳酸钠或碳酸氢钠,反应的离子方程式为CO2+H2O+SiO32—=CO32—+H2SiO3↓(或2CO2+2H2O+SiO32—=2HCO3—+H2SiO3↓),反应③是二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,反应的离子方程式为SiO2+2OH-=SiO32—+H2O;反应⑤是硅酸钠溶液与盐酸反应生成硅酸沉淀和氯化钠,反应的离子方程式为SiO32—+2H+=H2SiO3↓,故答案为:CO2+H2O+SiO32—=CO32—+H2SiO3↓(或2CO2+2H2O+SiO32—=2HCO3—+H2SiO3↓);SiO2+2OH-=SiO32—+H2O;SiO32—+2H+=H2SiO3↓。


科目:高中化学 来源: 题型:
【题目】以NA代表阿伏加德罗常数的数值,则关于热化学方程式C2H2(g)+![]() O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法中,正确的是( )
O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法中,正确的是( )
A. 转移10NA个电子时,该反应放出1300 kJ的能量
B. 生成NA个液态水分子时,吸收1300 kJ的能量
C. 有2NA个碳氧共用电子对生成时,放出1300 kJ的能量
D. 有10NA个碳氧共用电子对生成时,放出1300 kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是世界上最大的钨储藏国,金属钨可用于制造灯丝、合金钢和光学仪器,有“光明使者”的美誉;现以白钨矿(主要成分为CaWO4,还含有二氧化硅、氧化铁等杂质)为原料冶炼高纯度金属钨,工业流程如下:

已知:①钨酸酸性很弱,难溶于水;
②完全沉淀离子的pH值:SiO32-为8,WO42-为5;
③碳和金属钨在高温下会反应生成碳化钨。
回答下列问题:
(1)工业上生产纯碱常先制得碳酸氢钠,此法叫“联碱法”,为我国化工专家侯德榜创立,即向饱和食盐水中先通入NH3,再通入CO2,最终生成碳酸氢钠晶体和氯化铵溶液,写出该化学反应方程式:____________。
(2)流程中白钨矿CaWO4和纯碱发生的化学反应方程式是:________________________。
(3)滤渣B的主要成分是(写化学式)______。调节pH可选用的试剂是:_____(填选项)。
A.氨水 B.盐酸 C.NaOH溶液 D.Na2CO3溶液
(4)检验沉淀C是否洗涤干净的操作是________________________________________。
(5)为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而必须用氢气作还原剂的原因是_________。
(6)将氢氧化钙加入钨酸钠碱性溶液中可得到钨酸钙,已知某温度时,Ksp(CaWO4)=1×10-10,Ksp[Ca(OH)2]=4×10-7,当溶液中WO42-恰好沉淀完全(离子浓度等于10-5mol/L)时,溶液中c(OH-)=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制取二氧化硫并验证二氧化硫的某些性质的装置,试回答:
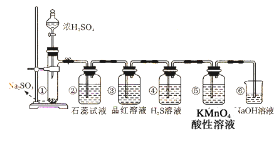
(1)在①中发生反应的化学方程式为_____________。
(2)②中的实验现象为紫色石蕊试液_________,此实验证明二氧化硫是_____气体。
(3)③中的品红溶液_________,证明二氧化硫有________性。
(4)④中的实验现象是______________,证明二氧化硫有__________性。
(5)⑤中的实验现象是________________,证明二氧化硫有____________性。
(6)⑥的作用是________,反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近日,中国科学家研发了一种碳修饰的镍基催化剂,实现了木质素选择性氢解得到酚类化合物。请回答下列问题:
(1)基态碳原子的核外电子有____种运动状态, 基态Ni原子的核外电子排布式为_________________。
(2)C、N、O三种元素的第一电离能由大到小的顺序为______________________。
(3)图1所示化合物中碳原子的杂化方式为_________,存在的化学键类型有_________(填标号)。

A.共价键 B.离子键 C.配位键 D.金属键 E.氢键
(4)碳的氧化物CO常作为许多金属配合物的配体,CO与N2互为等电子体,则CO分子中σ键与π键的个数比为______;测得熔点为170℃,预测属于___________晶体。
(5)一种储氢材料由镍、 镁元素组成,其晶胞结构如图2所示,则该晶体的化学式为__________,其晶胞边长为apm,列式计算晶胞密度为___________g/cm3 (不必计算出结果,阿伏加德岁常数的值为NA)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某兴趣小组根据教材实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验。请观察如下图所示实验装置,分析实验原理,并判断下列说法和做法,其中不科学的是( )

A. 甲为小苏打,乙为纯碱
B. 要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C. 加热不久就能看到A烧杯的澄清石灰水变浑浊
D. 整个实验过程中都没有发现A烧杯的澄清石灰水变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,利用冶铅废料(含有Pb、PbO、PbS、PbCO3、Pb(OH)2、C以及Fe及其氧化物等)制取立德粉(ZnS·BaSO4)和再提取铅的工艺流程如下:
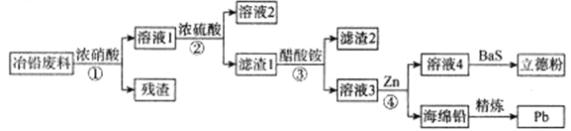
已知:
①醋酸铅易溶于水,难电离。
②常温下,Ksp(PbSO4)=1.6×10-8;Ksp(PbCO3)=8.0×10-14。
回答下列问题:
(1)为了加快①的反应速率,通常选用6mol/L的硝酸和60℃的反应条件,若温度继续升高,反而不利于反应的进行,原因可能是___________。
(2)步骤④若在实验室进行分离操作必需的玻璃仪器有___________,滤渣1的主要成分是硫酸铅,洗涤硫酸铅最好选用___________。
A.蒸馏水 B.苯 C.稀硫酸 D.饱和碳酸钠
(3)写出步骤③反应的离子方程式___________。
(4)采用电解法精炼铅,海绵铅连接电源的___________极(填正、负),生成铅的电极反应式为___________。
(5)处理含铅废料1t(含铅以PbO计,质量分数为11.15%),若回收率为90%,则得到的铅质量___________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右表为元素周期表前四周期的一部分,下列有关W、X、Y、Z、R五种元素的叙述中,正确的是( )
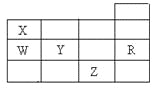
A. 常温下,Z单质为气态物质
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的氢化物的稳定性要比X的氢化物的稳定性强
D. Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101kPa时,有以下能量转化图,下列说法不正确的是( )

A. 转化Ⅱ的热化学方程式2CO(g)+O2(g)=2CO2(g) △H=-282.9 kJ·mol-1
B. 相同条件下,1mol C(s )和0.5 mol O2(g)总能量高于1mol CO(g)的能量
C. 由C→CO 的热化学方程式2C(s)+O2(g)=2CO(g) △H=-221.2 kJ·mol-1
D. CO2(g)分解为C(s)和O2(g)是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com