
纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:___________________________。
(2)写出“联合制碱法”有关反应的化学方程式:_______________________
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?_______________________。
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应列出计算原子利用率的表达式:原子利用率(%)=_________________。
(1)2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O
(2)NH3+CO2+H2O=NH4HCO3
NaCl+NH4HCO3=NaHCO3↓+NH4Cl
2NaHCO3 Na2CO3+H2O↑+CO2↑
Na2CO3+H2O↑+CO2↑
(3)“联合制碱法”中的CO2来源于合成氨厂,“氨碱法”中的CO2来源于煅烧石灰石
(4)  ×100%=49.77%
×100%=49.77%
【解析】氨碱法的原料:氯化钠、碳酸钙(或二氧化碳)及氨。
工艺流程:CaCO3 CaO+CO2↑CO2+NH3+H2O=NH4HCO3,
CaO+CO2↑CO2+NH3+H2O=NH4HCO3,
NaCl+NH4HCO3=NaHCO3↓+NH4Cl,2NaHCO3 Na2CO3+H2O↑+CO2↑,
Na2CO3+H2O↑+CO2↑,
CaO+H2O=Ca(OH)2,
产生CaCl2的反应:Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O,该反应的CaCl2中的Cl-来源于NaCl,Ca2+来源于CaCO3,产生无用的CaCl2,降低了NaCl的利用率。
CaCl2+2NH3↑+2H2O,该反应的CaCl2中的Cl-来源于NaCl,Ca2+来源于CaCO3,产生无用的CaCl2,降低了NaCl的利用率。
联合制碱法:NH3和CO2来源于合成氨厂
工艺流程:NH3+CO2+H2O=NH4HCO3,
NaCl+NH4HCO3=NaHCO3↓+NH4Cl,
2NaHCO3 Na2CO3+H2O↑+CO2↑。
Na2CO3+H2O↑+CO2↑。

依据总反应:2NaCl+CO2+H2O+2NH3=Na2CO3+2NH4Cl
可得:原子利用率= ×100%=49.77%。
×100%=49.77%。


科目:高中化学 来源:2014年高二化学人教版选修二 3.1 无机非金属材料练习卷(解析版) 题型:填空题
硅单质及其化合物应用很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下 :
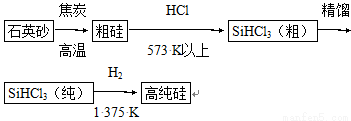
①写出由纯SiHCl3制备高纯硅的化学反应方程式____________________。
②整个制备过程必须严格控制无水、无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式____________________;H2还原SiHCl3过程中若混有O2,可能引起的后果是____________________。
(2)下列有关硅材料的说法正确的是 ( )。
A.单质硅化学性质稳定,但可以被强碱溶液腐蚀
B.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
C.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
D.光导纤维的主要成分是SiO2
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入盐酸,振荡。写出实验现象并给予解释(用化学方程式说明)_________________________ ____。
(4)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,这种材料是________(填字母)。
A.高温结构陶瓷 B.生物陶瓷 C.导电陶瓷
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 2.2 海水的综合利用练习卷(解析版) 题型:选择题
在氯碱工业中,原料盐中的杂质离子危害很高,能破坏离子膜,以下对Ca2+、Mg2+、Fe3+、SO42-除去顺序不合理的是 ( )。
A.BaCl2、NaOH、Na2CO3
B.BaCl2、Na2CO3、NaOH
C.NaOH、BaCl2、Na2CO3
D.Na2CO3、BaCl2、NaOH
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 1单元综合检测练习卷(解析版) 题型:选择题
有A、B、C、D四个中等城市,它们水源、能源充足,交通便利。它们相对地理位置如下图所示。各城市各有其特点:A城是风光秀丽,人口稠密,土地供应紧张的旅游城市,环保要求高,近郊有丰富的FeS2资源;B城是一个新兴的工业城市,已建有大型磷肥厂,土地供应充足。C城近郊有丰富的磷灰石资源,工业发达,但使用H2SO4的工业不多,土地供应充足;D城是一个古老的城市,它的周围是重要的农业区,是大量肥料的集散地。现拟建年产1×105 t硫酸的工厂,厂址应选在 ( )。
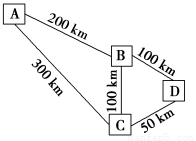
A.A城近郊 B.B城近郊 C.C城近郊 D.D城近郊
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 1.3 纯碱的生产练习卷(解析版) 题型:填空题
下图表示的是侯氏制碱法工艺流程示意图。
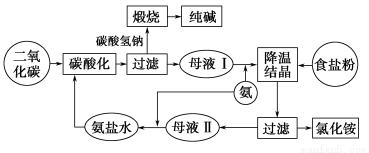
请回答:
(1)母液Ⅱ中所溶解的主要物质是________(写物质的化学式)。母液Ⅱ中含有低浓度的Na2CO3,主要原因是__________________________
(2)向母液Ⅱ中通入气体时要先通氨气后通二氧化碳气体,主要原因是_______________________________________
(3)母液Ⅰ和母液Ⅱ中都通入NH3。①NH3的主要来源是__________;②母液Ⅰ中通入NH3的主要目的是____________;③母液Ⅱ中通入NH3的主要目的是__________________。
(4)工艺流程的“煅烧→纯碱”处,可设计____________的循环。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 1.3 纯碱的生产练习卷(解析版) 题型:选择题
(1)1791年,法国医生路布兰首先获得制碱专利,以食盐、浓硫酸、石灰石、煤为原料制碱,该方法分三步:
①用NaCl与H2SO4反应制Na2SO4;2NaCl+H2SO4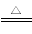 Na2SO4+2HCl↑
Na2SO4+2HCl↑
②用焦炭还原Na2SO4制Na2S;Na2SO4+4C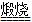 Na2S+4CO↑
Na2S+4CO↑
③用硫化钠与石灰石反应制Na2CO3;Na2S+CaCO3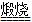 Na2CO3+CaS
Na2CO3+CaS
(2)下列说法正确的是 ( )。
A.②③两步都是氧化还原反应
B.只有第②步是氧化还原反应
C.该方法对生产设备基本没有腐蚀
D.该方法对环境污染较小
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 1.2 人工固氮合成氨练习卷(解析版) 题型:填空题
合成氨工业中,原料气(N2、H2、混有少量CO、NH3)在进入合成塔之前,常用醋酸二氨合铜(Ⅰ)溶液来吸收CO,其反应为CH3COO[Cu(NH3)2]+CO+NH3
CH3COO[Cu(NH3)3]·CO(正反应为放热反应)。
(1)必须除去CO的原因是___________________________。
(2)醋酸二氨合铜(Ⅰ)溶液吸收原料气中CO的适宜条件是______________________。
(3)吸收CO后的醋酸铜(Ⅰ)氨溶液经适当处理又可再生,恢复其吸收CO的能力而循环使用,其再生的条件是______________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 1.1 化工生产中的问题练习卷(解析版) 题型:选择题
你认为减少酸雨产生的途径可采取的措施是 ( )。
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加熟石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修一 4.3 垃圾资源化练习卷(解析版) 题型:选择题
倡导“免赠贺卡”、“免用一次性木筷”的出发点是( )。
A.减少个人经济支出 B.节约木材,保护森林
C.减少固体垃圾 D.移风易俗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com