

 ;I中所含化学键类型离子键、共价键,气体D所含元素在周期表中的位置第三周期ⅤⅡA族
;I中所含化学键类型离子键、共价键,气体D所含元素在周期表中的位置第三周期ⅤⅡA族分析 图中各物质是由1~20号元素中部分元素组成的单质或其化合物,D是一种黄绿色的气体单质,则D为Cl2,物质J可用于饮水消毒,反应④是化工生产中的重要反应,应是工业制备漂白粉原理,则I为Ca(OH)2、J为Ca(ClO)2、K为CaCl2,C是无色有刺激性气味的气体,反应⑤是实验室制备气体C,结合反应物与生成可知,为制备氨气的反应,故C为NH3、G为NH4Cl,结合转化关系可知H为HCl.F与水反应生成Ca(OH)2,则F为CaO,反应②是化工生产中的重要反应,为碳酸钙高温分解反应,故B为CaCO3、E为CO2.物质A由三种元素组成,1molA与水反应可生成1molB(CaCO3)和2molC(NH3),根据元素守恒可知A含有Ca、C、N三种元素,由原子守恒可知,A的化学式为CaCN2,据此解答.
解答 解:图中各物质是由1~20号元素中部分元素组成的单质或其化合物,D是一种黄绿色的气体单质,则D为Cl2,物质J可用于饮水消毒,反应④是化工生产中的重要反应,应是工业制备漂白粉原理,则I为Ca(OH)2、J为Ca(ClO)2、K为CaCl2,C是无色有刺激性气味的气体,反应⑤是实验室制备气体C,结合反应物与生成可知,为制备氨气的反应,故C为NH3、G为NH4Cl,结合转化关系可知H为HCl.F与水反应生成Ca(OH)2,则F为CaO,反应②是化工生产中的重要反应,为碳酸钙高温分解反应,故B为CaCO3、E为CO2.物质A由三种元素组成,1molA与水反应可生成1molB(CaCO3)和2molC(NH3),根据元素守恒可知A含有Ca、C、N三种元素,由原子守恒可知,A的化学式为CaCN2,
(1)E为CO2,其电子式为 ,I为Ca(OH)2,I中所含化学键类型为离子键、共价键,D为Cl2,气体D所含元素在周期表中的位置是第三周期ⅤⅡA族,
,I为Ca(OH)2,I中所含化学键类型为离子键、共价键,D为Cl2,气体D所含元素在周期表中的位置是第三周期ⅤⅡA族,
故答案为: ;离子键、共价键;第三周期ⅤⅡA族;
;离子键、共价键;第三周期ⅤⅡA族;
(2)G为NH4Cl,G的水溶液呈酸性,反应的离子方程式为NH4++H2O?NH3•H2O+H+,
故答案为:酸;NH4++H2O?NH3•H2O+H+;
(3)E为CO2,I为Ca(OH)2,反应的方程式为CO2+Ca(OH)2=CaCO3↓+H2O,
故答案为:CO2+Ca(OH)2=CaCO3↓+H2O;
(4)C为NH3,实验室制备气体C的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(5)含7.4g即0.1molCa(OH)2的稀溶液与200mL1mol/L的HCl溶液即含0.2molHCl,反应放出11.56kJ的热量,则1molCa(OH)2与2molHCl反应生成NH4Cl放出115.6kJ的热量,所以反应的热化学方程式为Ca(OH)2(aq)+2NH4Cl(aq)=CaCl2(aq)+2NH3↑(g)+2H2O(l)△H=-115.6kJ/mol,
故答案为:Ca(OH)2(aq)+2NH4Cl(aq)=CaCl2(aq)+2NH3↑(g)+2H2O(l)△H=-115.6kJ/mol;
(6)物质A由三种元素组成,1molA与水反应可生成1molCaCO3和2molNH3,根据元素守恒可知A含有Ca、C、N三种元素,由原子守恒可知,A的化学式为CaCN2,故答案为:CaCN2.
点评 本题考查无机物的推断,“D是黄绿色气体单质”是突破口,结合J的用途与中学常见的重要化工反应进行推断,侧重学生对元素化合物知识的熟练掌握考查,难度中等.


科目:高中化学 来源: 题型:解答题
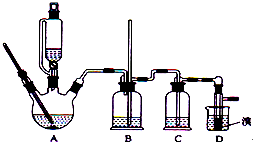 和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸 | B. | 烧碱溶液 | C. | AgNO3溶液 | D. | KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A. | 保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol•L-1,则反应的△H<0 | |
| B. | 若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变 | |
| C. | 保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.60 molCl2和0.60 molCO,反应达到平衡前的速率:v(正)>v(逆) | |
| D. | 保持其他条件不变,起始向容器中充入1.0 molCl2和0.8 molCO,达到平衡时,Cl2的转化率小于60% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 在NaCl晶体中,距Na+最近的Cl-形成正八面体 | |
| B. | 在CaF2晶体中,Ca2+、F-的配位数分别是4、8 | |
| C. | 在金刚石晶体中,碳原子与碳碳键个数的比为1:2 | |
| D. | 该气态团簇分子的分子式为EF或FE |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 分离方法 | 原理 |
| A | 除去Fe(OH)3胶体中的FeCl3 | 过滤 | 分散质微粒的大小不同 |
| B | 除去纯碱中的碳酸氢铵 | 加热 | 稳定性不同 |
| C | 分离KNO3和NaCl | 重结晶 | KNO3的溶解度大于NaCl |
| D | 分离食用油和汽油 | 分液 | 食用油和汽油的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | 3.4 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com