
【题目】己知镍的金属活动性介于铁和锡之间。工业上以氧化镍矿为原料制取高纯度的金属镍,最适宜的方法是
A. 氧化镍高温分解 B. 电解熔融的氧化镍
C. 高温下用焦炭还原氧化镍 D. 高温下用氢气还原氧化镍
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子。该小组同学取100mL水样进行实验,向水样中先滴加硝酸钡溶液,再滴加1 mol/L的硝酸,实验过程中沉淀质量的变化情况如图所示:

(1)水样中一定含有的阴离子是___________,其物质的量浓度之比为________。
(2)写出BC段所表示反应的离子方程式:___________________。
(3)由B点到C点变化过程中消耗硝酸的体积为________。
(4)试根据实验结果推断K+是否存在___________?(填“是”或“否”);若存在,K+的物质的量浓度c (K+)的范围是____________。(若K+不存在,则不必回答该问)
(5)设计简单实验验证原水样中可能存在的离子:_________(写出实验步骤、现象和结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等物质的量的铜片、铁片、铝片、银片分别置于4个小烧杯中,然后各加入足量的浓硝酸,放出NO2气体的体积最多的是
A. 银片 B .铁片 C.铜片 D.铝片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是( )

A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LNaOH溶液。整个实验过程中溶液的pH变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是

A. 实验过程中用pH试纸测定溶液的pH
B. a~b段,溶液中 C(H+)/C(OH-) 减小
C. b点对应溶液中:c(Cl-)>c(H+)>c(HClO)>c(ClO-)>c(OH-)
D. c点对应溶液中:c(Na+)=c(Cl-)+c(ClO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的组成与结构决定了物质的性质与变化,回答下列问题:
(1)量子力学把电子在原子核外的一个空间运动状态称为一个____________,电子除空间运动状态外,还有一种运动状态叫做____________。
(2)硒常用作光敏材料,基态硒原子的价电子排布式为_______________;与硒同周期的p区元素中第一电离能大于硒的元素有_________种。
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下图,As原子的杂化方式为___________,雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,写出该反应方程式________________。SnCl4分子的空间构型为_______。

(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图。

①储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱和面心则形成的储氢化合物的化学式为_________。
②测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为_______。(不必计算出结果,用NA表示阿伏伽德罗常数。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示实验室中常见的玻璃仪器,请回答下列有关问题。

(1)用仪器的字母填空:能用酒精灯直接加热的仪器是________,使用前要检查是否漏水的仪器有________,要分离汽油和水的混合物,应选择的仪器是________。
(2)b的名称是________。
(3)c常用于盛放固体试剂,实验室中下列试剂不能盛放其中的是________。
A.烧碱 B.锌粒 C.活性炭 D.石灰石
(4)下图是为完成相应实验的装置图,请分析指出其中一处错误。

A______________, B______________, C______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某非金属单质A和氧气发生化合反应生成B。B为气体,其体积是反应掉氧气体积的两倍(同温、同压)。以下对B的分子组成的推测一定正确的是( )
A. 有1个氧原子 B. 有2个氧原子
C. 有1个A原子 D. 有2个A原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学帮助水质检测站配制480 mL0.5mol·L- NaOH溶液以备使用。
(1)该同学应选择_______mL的容量瓶。
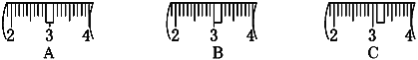
(2)该同学应称取NaOH固体_______g,用质量为23.1g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小_______ (填字母),并在下图中选出能正确表示游码位置的选项_______(填字母)。
附表:砝码规格
a | b | c | d | e | |
砝码大小/g | 100 | 50 | 20 | 10 | 5 |
(3)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会_____(填“偏大”、“偏小”或无影响,下同)
②容量瓶中原来有少量蒸馏水,浓度会_____。
(4)完成以下氧化还原反应的离子方程式:
______MnO![]() +______C2O
+______C2O![]() +______=_______Mn2++_______CO2↑+________。
+______=_______Mn2++_______CO2↑+________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com