
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:
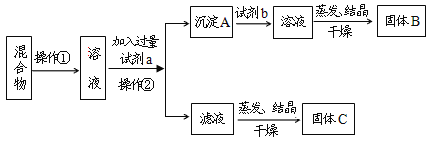
(1)操作①的名称是_____,操作②的名称是____。
(2)试剂a是_____(填化学式,下同),试剂b是____,固体B是_____。
(3)加入试剂a所发生反应的化学方程式为_______________________。加入试剂b所发生反应的化学方程式为_______________________。
【答案】溶解 过滤 K2CO3 HCl BaCl2 BaCl2 + K2CO3 = BaCO3↓ + 2KCl BaCO3 + 2HCl=BaCl2 + CO2↑+H2O
【解析】
分离KCl和BaCl2两种固体混合物,先溶于水配成溶液,然后加入过量K2CO3溶液使BaCl2完全转化为BaCO3沉淀,则试剂a为K2CO3溶液,过滤后BaCO3沉淀加入足量盐酸可生成BaCl2溶液,则试剂b为盐酸,在蒸发过程中过量的盐酸挥发,因此经蒸发、结晶、干燥后可得固体BaCl2;操作②所得滤液为KCl和K2CO3的混合物,应加入过量盐酸可得KCl溶液,经蒸发、结晶、干燥后可得固体KCl,据此进行分析。
(1)操作①是把KCl和BaCl2两种固体混合物溶于水,应为溶解;操作②是分离固体和液体的操作,应为过滤;
故答案为:溶解;过滤;
(2)固体溶解后加入过量K2CO3溶液使BaCl2转化为BaCO3沉淀,过滤后BaCO3沉淀加入足量的盐酸可生成BaCl2溶液,在蒸发过程中过量的盐酸挥发,经蒸发、结晶、干燥后可得固体BaCl2,故试剂a是K2CO3,试剂b是HCl,固体B是BaCl2;
故答案为:K2CO3;HCl;BaCl2;
(3)加入试剂a,K2CO3与BaCl2反应生成BaCO3沉淀和氯化钾,发生反应的化学方程式为:BaCl2 + K2CO3 = BaCO3↓ + 2KCl;加入试剂b,BaCO3与HCl生成二氧化碳、水和氯化钡,其反应的化学方程式为:BaCO3 + 2HCl=BaCl2 + CO2↑+H2O;
故答案为:BaCl2 + K2CO3 = BaCO3↓ + 2KCl;BaCO3 + 2HCl=BaCl2 + CO2↑+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)![]() Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图22所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图22所示。下列判断正确的是( )
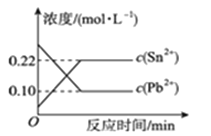
A. 往平衡体系中加入金属铅后,c(Pb2+)增大
B. 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C. 升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
D. 25 ℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.植物油、脂肪与氢氧化钠溶液反应均有甘油生成
B.甘氨酸既能与盐酸反应,又能与氢氧化钠溶液反应
C.淀粉和纤维素在一定条件下水解均可得到葡萄糖
D.鸡蛋清中加入饱和(NH4)2SO4溶液可使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡。根据所学知识回答下列问题:
(1)下列方法中可以使0.1mol/L CH3COOH溶液中c(H+)/c(CH3COOH)值增大的措施是_____
A.加水稀释 B.加入少量CH3COONa 固体
C.加入少量冰醋酸气体 D.通入少量HCl
(2)t℃时,水的离子积常数KW=1×10-12。
①该温度下,若100体积pH=a的H2SO4溶液与1体积pH=b的NaOH溶液等体积混合后溶液呈中性,则a+b=___________。
②该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因:_______________________________;该混合溶液中:c(A-)-c(Na+)= ________________mol/L(填准确数值)
(3)常温下,有浓度均为0.1mol/L的三种溶液:a.NaHCO3 b.NaClO c.CH3COONa
①三种溶液pH由大到小的顺序为:_______________(填序号)
②溶液a的pH大于8,则溶液中c(H2CO3)___ c(CO32―)(填“>” “<”或“=”)
(4)已知25℃时,Ksp(AgCl)= 1.8×10-10,现将足量氯化银分别放入:
a.100mL 蒸馏水中 b.100mL 0.2mol/L AgNO3 溶液中
c.100mL 0.1mol/L氯化铝溶液中 d.100mL 0.1mol/L盐酸溶液中
充分搅拌后,相同温度下银离子浓度由大到小的顺序是______________(填序号);b中氯离子浓度为_____________mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合物分离和提纯常用下图装置进行,按要求回答下列问题:
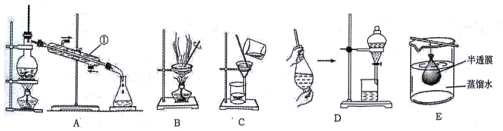
(1)仪器①的名称__________。
(2)除去澄清石灰水中悬浮的CaCO3颗粒应选用_______(填字母,下同)。
(3)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物应选用_______。
(4)用CCl4提取碘水中的碘单质应选用_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3mL酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
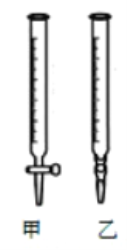
(1)以上步骤有错误的是(填编号)________。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入____中。(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:______(填编号)
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,滴定管尖嘴有气泡,滴定后无气泡
C.量取待测液的滴定管用蒸馏水洗涤后,未用待测液润洗
D.装标准溶液的滴定管滴定前仰视读数,滴定后俯视读
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com