
| A、①③ | B、①④ | C、②③ | D、②④ |
科目:高中化学 来源: 题型:
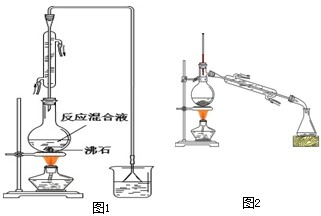
| 药品名称 | 熔点/℃ | 沸点(℃) | 密度 g/cm3 | 溶解性 |
| 正丁醇 | -89.5 | 117.7 | 0.8098 | 微溶于水、溶于浓硫酸 |
| 1-溴丁烷 | -112.4 | 101.6 | 1.2760 | 不溶于水和浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
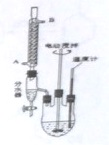 邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下:
邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molNa被完全氧化为Na2O2,失去的电子数为2NA |
| B、常温常压下,16gO3气体含有氧原子数为NA |
| C、常温常压下,22.4LCO2 含有分子数为NA |
| D、18g D2O所含有电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 在常温下,取pH=2的盐酸和醋酸溶液各100mL.向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图( )
在常温下,取pH=2的盐酸和醋酸溶液各100mL.向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图( )| A、曲线Ⅰ表示盐酸的pH变化 |
| B、曲线Ⅱ表示盐酸的pH变化 |
| C、在相同条件下,两溶液生成的气体体积相等 |
| D、醋酸溶液中加入锌的质量比盐酸溶液中多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com