
| A. | 组成蛋白质的氨基酸一定是α-氨基酸 | |
| B. | 氨基酸都含有手性碳原子 | |
| C. | 氨基酸具有两性,蛋白质不具有两性 | |
| D. | 天然氨基酸大部分能溶于水,难溶于乙醇、乙醚 |
分析 A.脯氨酸含有亚氨基,其余大部分含有a-氨基;
B.手性碳是指碳原子所连的4个基团都不一样;
C.氨基酸以及蛋白质中含有氨基和羧基;
D.氨基酸都是极性比较大的分子.
解答 解:A.脯氨酸含有亚氨基,其余大部分含有a-氨基,组成蛋白质的氨基酸不一定是α-氨基酸,故A错误;
B.氨基酸不一定含有手性碳原子,故B错误;
C.氨基酸以及蛋白质中含有氨基和羧基,既能和酸反应,又能与碱反应,故C错误;
D.氨基酸都是极性比较大的分子,物质性质相近相溶的原理,水是一种极性很大的溶剂,所以氨基酸溶易于水而不易溶于乙醇和乙醚,故D正确.
故选D.
点评 本题考查氨基酸、蛋白质的结构和性质特点,难度不大,注意脯氨酸含有亚氨基,其余大部分含有a-氨基,氨基酸都是极性比较大的分子.


科目:高中化学 来源: 题型:解答题
| 试剂 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) | 溶解性 | ||
| 水 | 乙醇 | 乙醚 | ||||
| 1-苯乙醇 | 20 | 203.4 | 1.013 | 不溶 | 溶 | 溶 |
| 苯乙酮 | 19.7 | 202.3 | 1.028 | 不溶 | 溶 | 溶 |
| 硼氢化钠 | - | - | 1.076 | 溶 | 溶 | 不溶 |
| 乙醚 | -116.3 | 34.6 | 0.713 | 微溶 | 溶 | - |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A. | 保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol•L-1,则反应的△H<0 | |
| B. | 若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变 | |
| C. | 保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.60 molCl2和0.60 molCO,反应达到平衡前的速率:v(正)>v(逆) | |
| D. | 保持其他条件不变,起始向容器中充入1.0 molCl2和0.8 molCO,达到平衡时,Cl2的转化率小于60% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3 | B. | 0.3 mol/(L•s) | C. | 0.4 mol(L•s)-1 | D. | 0.04 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 在NaCl晶体中,距Na+最近的Cl-形成正八面体 | |
| B. | 在CaF2晶体中,Ca2+、F-的配位数分别是4、8 | |
| C. | 在金刚石晶体中,碳原子与碳碳键个数的比为1:2 | |
| D. | 该气态团簇分子的分子式为EF或FE |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的化学性质比乙烷活泼 | |
| B. | 乙烯燃烧时,火焰明亮,同时伴有黑烟 | |
| C. | 乙烯使酸性高锰酸钾溶液褪色是由于发生了氧化反应 | |
| D. | 乙烯分子的双键中的一个键可以断裂,容易发生加成反应和取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
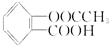 )与足量的NaOH溶液反应,最多消耗NaOH的物质的量为( )
)与足量的NaOH溶液反应,最多消耗NaOH的物质的量为( )| A. | 1.5mol | B. | 2 mol | C. | 1 mol | D. | 0.5 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com