
判断正误,正确的划“√”,错误的划“×”
(1)铝罐可久盛食醋( )
(2014·福建理综,6C)
(2)氢氧化铝可作胃酸的中和剂( )
(2014·四川理综,1D)
(3)明矾用作净水剂不涉及化学变化( )
(2014·重庆理综,1A)
(4)铝与Fe2O3发生铝热反应,反应后固体物质增重( )
(2014·新课标全国卷Ⅱ,9C)
(5)AlCl3溶液中加入过量稀氨水:Al3++3NH3·H2O===Al(OH)3↓+4NH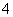 ( )
( )
(2014·四川理综,3C改编)
(6)Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O===2AlO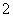 +3H2↑( )
+3H2↑( )
(2014·北京理综,9D)
(7)明矾溶液中滴入Ba(OH)2溶液使SO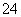 恰好完全沉淀:2Ba2++3OH-+Al3++2SO
恰好完全沉淀:2Ba2++3OH-+Al3++2SO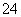 ===2BaSO4↓+Al(OH)3↓( )
===2BaSO4↓+Al(OH)3↓( )
(2013·大纲全国卷,11D)
科目:高中化学 来源: 题型:
化合物A、B是中学常见的物质,其阴、阳离子只能从下表中选择:
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH |
| 阴离子 | OH-、NO |
(1)若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性。混合后产生不溶于稀盐酸的白色沉淀及能使湿润的红色石蕊试纸变蓝色的气体。
①B的化学式为______________。
②A、B溶液混合加热反应的离子方程式为________________________________________________________________________。
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则
①A的化学式为______________。
②经分析上述过程中溶液变黄的原因可能有两种(用离子方程式表示)
Ⅰ________________________________________________________________________;
Ⅱ________________________________________________________________________。
③请用一简易方法证明上述溶液变黄的原因________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铝土矿的主要成分为氧化铝、氧化铁和二氧化硅,工业上经过下列工艺可以冶炼金属铝:


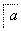

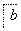 ,③
,③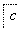 ,④
,④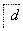 电解,
电解,
下列说法中错误的是( )
A.①②中除加试剂外,还需要进行过滤操作
B.a、b中铝元素的化合价相同
C.③中需要通入过量的氨气
D.④进行的操作是加热,而且d一定是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.铝制容器可盛装热的浓硫酸
B.镁的金属性比铝的金属性强
C.氢氧化铝能溶于过量氨水
D.镁在空气中燃烧生成的固体只有MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、NH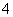 、Mg2+、Al3+、Fe3+、CO
、Mg2+、Al3+、Fe3+、CO 、SO
、SO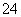 、NO
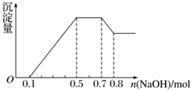
、NO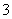 中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中n(NH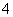 )=0.2 mol
)=0.2 mol
C.溶液中一定不含CO ,可能含有SO
,可能含有SO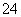 和NO
和NO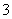
D.n(H+)∶n(Al3+)∶n(Mg2+)=2∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
处于前三周期的主族元素A、B、C、D,其离子半径逐渐增大,它们的原子中核外都有一个未成对电子。已知A和D处于同一周期,0.2 mol A单质可以从D的氢化物的水溶液中置换出6.72 L H2(标准状况),试回答:
(1)写出元素符号:
A.________,B.________,C.________,D.________;
(2)若C有气态氢化物存在,比较C和D的氢化物:
沸点__________,稳定性__________,水溶液的酸性____________;
(3)四种元素的第一电离能由大到小的排列顺序是________________________;
(4)四种元素的电负性由小到大的顺序是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com