
【题目】下列会引起中毒甚至死亡的是
①用工业酒精兑水假冒白酒 ②用福尔马林浸泡海参使食物保鲜
③用无碘盐假冒碘盐 ④用亚硝酸钠假冒食盐
⑤用盛过农药的桶装工业用油假冒食用油
A. ①②③④ B. ①②④⑤ C. ②③④⑤ D. ①③④⑤
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】现有两种淀粉酶A与B,某小组为探究不同温度条件下这两种淀粉酶的活性,做了如下探究实验。
实验过程:
组别 步骤 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Ⅰ.设置水浴缸温度/℃ | 20 | 30 | 40 | 50 | 20 | 30 | 40 | 50 |
Ⅱ.取8只试管各加入淀粉溶液/mL,分别保温5 min | 10 | 10 | 10 | 10 | 10 | 10 | 10 | 10 |
Ⅲ.另取8只试管各加入等量淀粉酶溶液,分别保温5 min | 酶A | 酶A | 酶A | 酶A | 酶A | 酶A | 酶A | 酶A |
Ⅳ.将同组两个试管中的淀粉溶液与淀粉酶溶液混合摇匀,保温5 min | ||||||||
实验结果:对各组淀粉含量进行检测,结果如图所示。
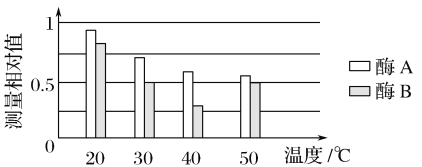
(1)该实验的自变量是________,无关变量有________(至少写出2种)。
(2)根据实验结果分析,酶A在________℃条件时活性较高。
(3)此实验通过检测淀粉的剩余量来表示酶的活性,不能用斐林试剂检测生成物麦芽糖的含量来表示,说明理由:________________。
(4)若要进一步探究酶B的最适温度,实验设计的主要思路应是:在________℃之间设立较小等温度梯度的分组实验,按上述步骤进行实验,分析结果得出结论。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaHSO3被用于棉织物和有机物漂白以及在染料、造纸、制革等工业中用作还原剂。
(1)NaHSO3可由NaOH溶液吸收SO2制得。
2NaOH(aq)+SO2(g)==Na2SO3(aq)+H2O(l) ΔH1
2NaHSO3(aq)==Na2SO3(aq)+SO2(g)+H2O(l) ΔH2
则反应SO2(g)+NaOH(aq)==NaHSO3(aq)的ΔH3=__________(用含ΔH1、ΔH2的代数式表示)。
(2)NaHSO3在不同温度下均可被KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3 的反应速率。将浓度均为0.020mol·L-1NaHSO3(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。

①a点时,v(NaHSO3)=__________mol·L-1·s-1。
②10~40℃区间内,显色时间越来越短,其原因是__________。
(3)已知:t℃时 H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7;NaHSO3溶液pH<7。在t℃时,往NaOH溶液中通入SO2。
①在NaHSO3溶液中加入少量下列物质后,c(H2SO3)/c(HSO3-)的值增大的是______(填字母);
A.H2O B.稀H2SO4 C.H2O2溶液 D.NaOH溶液
②某时刻,测得溶液的pH=6,则此时,n(HSO3-)/n(SO32-)=_________;
③请画出从开始通入SO2直至过量时,溶液中n(SO32-)∶n(HSO3-)随pH的变化趋势图。_______

(4)以硝酸、硫酸水溶液作电解质进行电解,在汞电极上NO3-可转化为NH2OH,以铂为另一极,则该电解反应的化学方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左侧充入1 mol N2,右侧充入CO和CO2的混合气体共8 g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是

A. 右侧CO与CO2分子数之比为1∶3
B. 右侧气体密度是相同条件下氢气密度的18倍
C. 右侧CO的质量为1.75 g
D. 若隔板处于距离右端1/6处,其他条件不变,则前后两次压强之比为25∶24
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 在医药合成中有着广泛的用途。下列而关该物质的说法正确的是
在医药合成中有着广泛的用途。下列而关该物质的说法正确的是
A. 该化含物中含氧官能团为酯基
B. 该化台物中的所有碳原子一定处于同一平面内
C. 该化合物可发生取代反应、加成反应和氧化反应
D. 该化合物的同分异构体中,苯环上有两个取代基的共3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“铜都”安徽铜陵有许多黄铜矿(主要成分为CuFeS2,含少量Al2O3、SiO2),黄铜矿是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)火法炼铜首先要焙烧黄铜矿,其反应原理为2CuFeS2+O2![]() Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,若反应中转移0.3mol电子时,则标准状况下,产生SO2的体积为________L。
Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,若反应中转移0.3mol电子时,则标准状况下,产生SO2的体积为________L。
(2)焙烧黄铜矿产生的Cu2S可被稀硝酸氧化为Cu2+ 和硫单质,HNO3的还原产物为NO,试写出Cu2S与稀硝酸反应的离子方程式,并用双桥式表示电子转移__________________。
(3)焙烧黄铜矿还可得到Cu2O,将21.6g Cu2O加入到500mL某浓度的稀硝酸中,固体物质完全反应,生成Cu(NO3)2和NO,在所得溶液中加入1.0molL-1的NaOH溶液1.0L,此时溶液呈中性。原硝酸的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 浓度均为0.1mol/L (NH4)2SO4、NH4HSO4混和溶液中滴加0.1mol/L的Ba(OH)2溶液。充分反应后静置,溶液的pH 与所加Ba(OH)2溶液体积的关系如右图,下列说法正确的是

A. a点溶液中: c(NH4+) +c(NH3·H2O)=0.2 mol/L
B. b点溶液中: c(NH4+)>c(SO42-)>c(H+)> c(NH3·H2O)> c(OH-)
C. c点溶液中: c(Ba2+)+ c(NH4+)= c(SO42-)
D. d 点溶液中: c(NH3·H2O)> c(SO42-)>c(NH4+)> c(OH-)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述中正确的是( )
A.钠块沉在乙醇液面之下
B.钠块熔化成小球
C.钠块在乙醇的液面上游动
D.向烧杯中滴入几滴酚酞溶液变红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com