
A.溶液的浓度变为0.08 mol·L-1 B.阳极上产生112 mL O2(标准状况)
C.转移的电子数是1.204×1022 D.反应中有0.02 mol的Ag被氧化
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
①A和E溶液显碱性,0.1 mol·L-1A溶液的pH小于13。
②在B溶液中逐滴加入氯水有白色沉淀生成,继续加氨水至过量,沉淀消失。
③在C溶液中加入铁粉,溶液的质量增加。
④在D溶液中加入过量Ba(OH)2溶液,没有沉淀。
(1)根据以上事实推断:A是_________,B是_________,C是_________,D是_________,E是_________。
(2)写出实验②中有关反应的离子方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
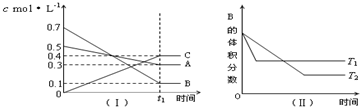
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1 ②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1 ③2 s时物质A的转化率为70 % ④2 s时物质B的浓度为0.7 mol·L-1
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
①用物质A表示的反应的平均速率为0.3 mol·(L·s)-1
②用物质B表示的反应的平均速率为0.6 mol·(L·s)-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol·L-1
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com