
| V |
| Vm |
| 2.24L |
| 22.4L/mol |
| 6.5g |
| 13g |


科目:高中化学 来源: 题型:
| A、稀硫酸和氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
| B、钠和水反应:Na+2H2O═Na++2OH-+H2↑ |
| C、氢氧化铝治疗胃酸过多:OH-+H+═H2O |
| D、用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 按要求对如图中两极进行必要的连接并填空:
按要求对如图中两极进行必要的连接并填空:查看答案和解析>>
科目:高中化学 来源: 题型:
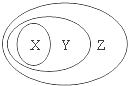 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )| X | Y | Z | |
| A | 氧化物 | 化合物 | 纯净物 |
| B | 盐 | 离子化合物 | 化合物 |
| C | 胶体 | 分散系 | 混合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com