

| A. | 锌电极发生还原反应:铜电极发生氧化反应 | |
| B. | 铜电极做正极发生的电极反应为:2H++2e-═H2↑ | |
| C. | 当有13g Zn溶解时,电路中就有0.5mol电子通过 | |
| D. | 电子从锌电极通过电流表流向铜电极 |
分析 图为铜锌原电池,原电池工作时,锌为负极,发生氧化反应,电极反应为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应为Cu2++2e-=Cu,电子由负极经外电路流向正极,溶液中阳离子向正极移动,阴离子向负极移动,结合电极方程式解答该题.
解答 解:A.锌为负极,发生氧化反应,铜为正极,发生还原反应,故A错误;
B.电解质为硫酸铜,正极反应为Cu2++2e-=Cu,故B错误;
C.n(Zn)=$\frac{13g}{65g/mol}$=0.2moL,电极反应为Zn-2e-=Zn2+,可知转移电子0.4mol,故C错误;
D.原电池工作时,锌为负极,铜为正极,电子从锌电极通过电流表流向铜电极,故D正确.
故选D.
点评 本题考查原电池反应,题目难度不大,注意根据金属的活泼性强弱判断原电池的正负极反应,能正确书写电极反应式,理解原电池的工作原理.


科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①②③ | C. | ①④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非自发进行的反应一定不能发生 | |
| B. | 在一定条件下,非自发进行的反应也能进行 | |
| C. | 自发进行的反应一定迅速 | |
| D. | 凡是熵增加的过程都是自发过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5mol•L-1•min-1 | B. | v(B)=0.3mol•L-1•s-1 | ||
| C. | v(C)=0.1mol•L-1•s-1 | D. | v(D)=0.4mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
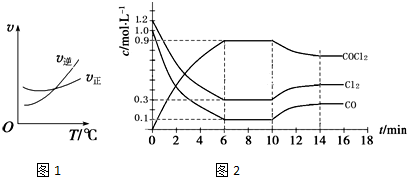
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加催化剂同时升高温度 | B. | 降低温度同时增大压强 | ||
| C. | 充入CO | D. | 加催化剂同时增大压强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com