

 ;
;分析 A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1:1,但I晶体中阴、阳离子个数比是2:1,I常用作干燥剂,A、B都能与水反应,且A与水反应生成C能点燃生成水,可以推得A应为CaC2,C为C2H2,所以D为Ca(OH)2,C在E中点燃生成K和水,所以E为O2,K为CO2,B和水反应生成D和E,则B为CaO2,N和J反应生成G是白烟,则G为NH4Cl,氢氧化钙与氯化铵加热生成氨气、氯化钙和水,所以J为NH3,I为CaCl2,反应③在工业上有一个重要用途,应为氯气与氢氧化钙制漂白粉的反应,所以F为Cl2,H为Ca(ClO)2,次氯酸钙与二氧化碳生成L和M,L能见光分解生成E和N,所以L为HClO,M为CaCO3,N为HCl,符合各物质的转化关系,据此答题.
解答 解:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1:1,但I晶体中阴、阳离子个数比是2:1,I常用作干燥剂,A、B都能与水反应,且A与水反应生成C能点燃生成水,可以推得A应为CaC2,C为C2H2,所以D为Ca(OH)2,C在E中点燃生成K和水,所以E为O2,K为CO2,B和水反应生成D和E,则B为CaO2,N和J反应生成G是白烟,则G为NH4Cl,氢氧化钙与氯化铵加热生成氨气、氯化钙和水,所以J为NH3,I为CaCl2,反应③在工业上有一个重要用途,应为氯气与氢氧化钙制漂白粉的反应,所以F为Cl2,H为Ca(ClO)2,次氯酸钙与二氧化碳生成L和M,L能见光分解生成E和N,所以L为HClO,M为CaCO3,N为HCl,符合各物质的转化关系,
(1)I为CaCl2,I的电子式是 ,
,
故答案为: ;
;
(2)反应⑥为二氧化碳与次氯酸钙反应生成次氯酸和碳酸钙,反应的化学方程式是Ca(ClO)2+CO2+H2O=CaCO3+2HClO,反应③在工业上的一个重要用途是制漂白粉或漂白精,
故答案为:Ca(ClO)2+CO2+H2O=CaCO3+2HClO;制漂白粉或漂白精;
(3)反应④是实验室制氨气的反应,反应的化学方程式是 2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(4)燃烧热实指1ml可燃物燃烧生成最稳定的氧化物释放出的能量,所以乙炔燃烧的方程式为:C2H2(g)+$\frac{5}{2}$ O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol,
故答案为:C2H2(g)+$\frac{5}{2}$ O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol;
(5)根据上面的分析可知,B的化学式是CaO2,
故答案为:CaO2.
点评 本题是一道框图推断题,考查知识面较广,要求学生具有分析和解决问题的能力,难度较大.


科目:高中化学 来源: 题型:多选题
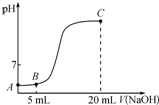 常温下,向10mL 0.1mol•L-1的CH3COOH溶液中逐滴加入0.1mol•L-1 NaOH溶液,所得滴定曲线如图所示.下列说法一定正确的是( )
常温下,向10mL 0.1mol•L-1的CH3COOH溶液中逐滴加入0.1mol•L-1 NaOH溶液,所得滴定曲线如图所示.下列说法一定正确的是( )| A. | A点的pH为1 | |
| B. | B点时:2c(H+)+c(CH3COOH)═2c(OH-)+c(CH3COO-) | |
| C. | 在A→B之间:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | C点时:c(H+)+c(Na+)═c(OH-)+c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①中氧化剂是氧气和水 | |
| B. | 钢铁在潮湿的空气中不能发生电化学腐蚀 | |
| C. | 反应①、②中电子转移数目相等 | |
| D. | 与铜质水龙头连接处的钢质水管不易发生腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ③④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 393.5kJ | B. | 983.75KJ | C. | 1075.5kJ | D. | 1185.5KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H-2个氢原子 | |
| B. | Mg2+-镁元素的化合价为+2 | |
| C. | N2-2个氮原子 | |
| D. | $\stackrel{+2}{Ca}$2+一个钙离子带有2个单位的正电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 气体E呈红棕色,不能直接排放 | |
| B. | 溶液S中所含溶质、沉淀R都可用作药物 | |
| C. | 合金样品中Al的质量分数为$\frac{9a}{17c}$×100% | |
| D. | 合金样品中Cu的质量分数为$\frac{a-b-c}{a}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学能与电能的相互转化必须通过一定的装置 | |
| B. | 任何化学反应都伴随有能量的变化 | |
| C. | 能源的开发和利用情况可以衡量一个国家或地区的经济发展和科学技术水平 | |
| D. | 太阳能、风能、氢能、电能都是可再生的新能源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com