
·ÖĪö £Ø1£©ĢāÖŠŹµŃéÉę¼°ČÜŅŗµÄĮæČ””¢ŻĶČ”ŗĶ·ÖŅŗµČ²Ł×÷£»
£Ø2£©·ÖŅŗŹ±Ó¦×¢Ņā±ÜĆāÉĻ²ćŅŗĢå“ÓĻĀ¶ĖĮ÷³ö£»
£Ø3£©Ź¹ÓĆ·ÖŅŗĀ©¶·£¬Ó¦¼ģ²é²£Į§Čū“¦ŗĶĘææŚ“¦£»ŻĶČ”Ź±£¬ŻĶČ”¼ĮÓėĖ®»„²»ĻąČÜ£»ĒŅÓĆÕōĮóµÄ·½·Ø½ųŅ»²½·ÖĄėµāŗĶĖÄĀČ»ÆĢ¼£®
½ā“š ½ā£ŗ£Ø1£©ĢāÖŠŹµŃéÉę¼°ČÜŅŗµÄĮæČ””¢ŻĶČ”ŗĶ·ÖŅŗµČ²Ł×÷£¬æÉÓƵ½ÉÕ±”¢½ŗĶ·µĪ¹Ü”¢ĮæĶ²µČ£¬²»ÓĆ²£Į§°ō£¬¹Ź“š°øĪŖ£ŗB£»
£Ø2£©·ÖŅŗŹ±Ó¦×¢Ņā±ÜĆāÉĻ²ćŅŗĢå“ÓĻĀ¶ĖĮ÷³ö£¬×¢ŅāŃŪ¾¦×¢ŹÓ¶ž²ćŅŗĢå·Ö½ēĆę£¬µ±ĶźČ«·ÖæŖŹ±£¬¼°Ź±¹Ų±ÕŠżČū£¬
¹Ź“š°øĪŖ£ŗŃŪ¾¦×¢ŹÓ¶ž²ćŅŗĢå·Ö½ēĆę£¬µ±ĶźČ«·ÖæŖŹ±£¬¼°Ź±¹Ų±ÕŠżČū£»
£Ø3£©A£®Ź¹ÓĆ·ÖŅŗĀ©¶·£¬Ó¦¼ģ²é²£Į§Čū“¦ŗĶĘææŚ“¦£¬¹ŹA“ķĪó£»
B£®ĖÄĀČ»ÆĢ¼ĆܶȱČĖ®“ó£¬ŻĶČ”ŗó·ÖŅŗĀ©¶·ÄŚ¹Ū²ģµ½µÄĻÖĻóŹĒŅŗĢå·Ö¶ž²ć£¬ÉĻ²ć½Ó½üĪŽÉ«£¬ĻĀ²ć×ĻŗģÉ«£¬¹ŹBÕżČ·£»
C£®æÉŅŌÓɱ½“śĢęĖÄĀČ»ÆĢ¼£¬µ«²»æÉŅŌÓĆŅŅ“¼£¬ŅņŅŅ“¼ÓėĖ®»ģČÜ£¬¹ŹCÕżČ·£»
D£®µāŗĶĖÄĀČ»ÆĢ¼µÄ·Šµć²»Ķ¬£¬æÉŅŌ²ÉÓĆÕōĮóµÄ·½·ØĄ“½ųŅ»²½·ÖĄėµāŗĶĖÄĀČ»ÆĢ¼£¬¹ŹDÕżČ·£®
¹Ź“š°øĪŖ£ŗBCD£®
µćĘĄ ±¾Ģāæ¼²é½Ļ×ŪŗĻ£¬²ąÖŲ»ģŗĻĪļµÄ·ÖĄė”¢Ģį“æ¼°ŹµŃéŅĒĘ÷”¢ŹµŃé²½ÖčµÄ漲飬°ŃĪÕĪļÖŹµŲŠŌÖŹÓė·ÖĄėŌĄķ”¢ŻĶČ”²Ł×÷µÄ²½ÖčĪŖ½ā“šµÄ¹Ų¼ü£¬×¢ÖŲ»ł“”ÖŖŹ¶ŗĶŹµŃ黳±¾¼¼ÄܵÄѵĮ·£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹żĀĖ | B£® | ÉųĪö | C£® | ŻĶČ” | D£® | Õō·¢½į¾§ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | AgClŌŚ±„ŗĶNaClČÜŅŗÖŠµÄKsp±ČŌŚ“æĖ®ÖŠµÄŠ” | |
| B£® | AgClµÄŠü×ĒŅŗÖŠc£ØCl-£©=4”Į10-5.5mol/L | |
| C£® | ½«0.001 mol•L-1AgNO3ČÜŅŗµĪČė0.001 mol•L-1µÄKCl£¬ĪŽ³ĮµķĪö³ö | |
| D£® | ĻņAgClµÄŠü×ĒŅŗÖŠ¼ÓČėNaBrČÜŅŗ£¬°×É«³Įµķ×Ŗ»ÆĪŖµ»ĘÉ«£¬ĖµĆ÷Ksp£ØAgCl£©£¼Ksp£ØAgBr£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗ£¬ĻņČŻĮæĘæ¼ÓĖ®ÖĮĄėæĢ¶ČĻß1”«2cm£¬øÄÓĆ½ŗĶ·µĪ¹Ü¶ØČŻ | |
| B£® | ÓĆŅ©³×»ņÕßÖ½²Ū°Ń·ŪĩדŅ©Ę·ĖĶČėŹŌ¹ÜµÄµ×²æ | |
| C£® | ÓĆ½ą¾»µÄ²¬ĖæÕŗČ”“ż²āŅŗ£¬ÖĆÓŚ»šŃęÉĻ×ĘÉÕ£¬Ķø¹żĄ¶É«īܲ£Į§ÄܹŪ²ģµ½»šŃę³Ź×ĻÉ«£¬øĆČÜŅŗÖŠŅ»¶Øŗ¬ÓŠ¼ŲĄė×Ó£¬²»ŗ¬ÓŠÄĘĄė×Ó | |
| D£® | ·ÖŅŗ²Ł×÷£¬·ÖŅŗĀ©¶·ÖŠĻĀ²ćŅŗĢå“ÓĻĀæŚ·Å³ö£¬ÉĻ²ćŅŗĢå“ÓÉĻæŚµ¹³ö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| X | Y | ||
| Z | W |
| A£® | YŌŖĖŲ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ»ÆѧŹ½ĪŖH3YO4 | |
| B£® | Ō×Ó°ė¾¶ÓÉŠ”µ½“óµÄĖ³ŠņĪŖ£ŗX£¼Y£¼W£¼Z | |
| C£® | ÓėĶ¬ÅØ¶ČµÄŃĪĖį·“Ó¦£¬Z±ČWøü¾ēĮŅ | |
| D£® | XµÄĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ±ČYµÄøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5.6g | B£® | 16.8g | C£® | 11.2g | D£® | 33.6g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
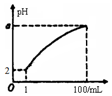 pH=2µÄČõĖįHAČÜŅŗ1mL£¬¼ÓĖ®Ļ”ŹĶµ½100mL£¬ĘäpHÓėČÜŅŗĢå»ż£ØV£©µÄ¹ŲĻµČēĶ¼Ź¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
pH=2µÄČõĖįHAČÜŅŗ1mL£¬¼ÓĖ®Ļ”ŹĶµ½100mL£¬ĘäpHÓėČÜŅŗĢå»ż£ØV£©µÄ¹ŲĻµČēĶ¼Ź¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | aµÄȔֵ·¶Ī§ĪŖ2£¼a£¼4 | |
| B£® | HAČÜŅŗ¼ÓČČŹ±£¬ČÜŅŗĖįŠŌŌöĒæ | |
| C£® | ÓėpH=12µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗóČÜŅŗµÄpH=7 | |
| D£® | HAČÜŅŗÓėNaOHČÜŅŗĒ”ŗĆĶźČ«·“Ó¦Ź±£¬c£ØNa+£©£¾c£ØA-£©£¾c£ØOH-£©£¾c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓČČĒ°ŗóŅ»Ńł¶ą | B£® | ¼ÓČČĒ°ĻūŗĵĶą | ||
| C£® | ¼ÓČČŗóĻūŗĵĶą | D£® | µ±Na2O2ŹŹĮæŹ±²Å»įŅ»Ńł¶ąĪŽ·Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 25”ꏱ£¬Ļņ10mL 0.1mol•L-1 NH4HSO4ČÜŅŗÖŠÖšµĪµĪČė0.1mol•L-1 NaOHČÜŅŗ£¬ČÜŅŗµÄpHÓėNaOHČÜŅŗĢå»ż¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
25”ꏱ£¬Ļņ10mL 0.1mol•L-1 NH4HSO4ČÜŅŗÖŠÖšµĪµĪČė0.1mol•L-1 NaOHČÜŅŗ£¬ČÜŅŗµÄpHÓėNaOHČÜŅŗĢå»ż¹ŲĻµČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com