
 25°C时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)
25°C时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)  Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
D.25°C时,该反应的平衡常数K=2.2
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
对于密闭容器中的可逆反应:mX(g)+nY(s)  pZ(g) ΔH<0,达化学平衡后,改变条件,下列表述不正确的是( )
pZ(g) ΔH<0,达化学平衡后,改变条件,下列表述不正确的是( )
A.增大压强,化学平衡不一定发生移动
B.通入氦气,化学平衡不一定发生移动
C.增加X或Y的物质的量,化学平衡一定发生移动
D.其他条件不变,升高温度,化学平衡一定发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
光刻胶是制大规模集成电路、印刷电路板和激光制板技术中的关键材料。某一肉桂酸型光刻胶的主要成分A经光照固化转变为B。


(1)请指出A中含有的官能团:________(填两种)。
(2)A经光照固化转变为B,发生了________反应(填反应类型)。
(3)写出A与NaOH溶液反应的化学方程式:____________
___________________________________________________。
(4)写出B在酸性条件下水解得到的芳香族化合物的分子式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g)  4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
A.该反应的化学平衡常数表达式是K=
B.此时,B的平衡转化率是40%
C.增大该体系的压强,化学平衡常数增大
D.增加B,A的平衡转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
2N2O5(g)  4NO2(g)+O2(g) ΔH>0
4NO2(g)+O2(g) ΔH>0
T1温度下的部分实验数据为:
| t/s | 0 | 500 | 1 000 | 1 500 |
| c(N2O5)/mol/ L | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是( )
A.500 s内N2O5分解速率为2.96×10-3 mol/(L·s)
B.T1温度下的平衡常数为K1=125,1 000 s时转化率为50%
C.其他条件不变时,T2温度下反应到1 000 s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
查看答案和解析>>
科目:高中化学 来源: 题型:
为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化剂作用下,通过下列反应:CCl4+H2 CHCl3+HCl使CCl4转
CHCl3+HCl使CCl4转 化为重要的化工原料氯仿(CHCl3)。此反应伴随有副反应,会生成CH2Cl2、CH3Cl
化为重要的化工原料氯仿(CHCl3)。此反应伴随有副反应,会生成CH2Cl2、CH3Cl 和CH4等。已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃。
和CH4等。已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃。
(1)在密闭容器中,该反应达到平衡状态后,测得如下数据(假设不考虑副反应)。
| 实验序号 | 温度℃ | 初始CCl4浓度(mol/L) | 初始H2浓度(mol/L) | CCl4的平衡转化率 |
| 1 | 110 | 0.8 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | B |
①此反应的化学平衡常数表达式为________________,在110℃时平衡常数为____________。
②实验1中,CCl4的转化率A__________50%(填“大于”、“小于”或“等于”)。
③实验2中,10 h后达到平衡,H2的平均反应速率为__________。
④实验3中,B的值________(选填序号)。
A.等于50% B.大于50%
C.小于50% D.从本题资料无法判断
(2)120℃时,在相同条件的密闭容器中,分别进行H2的初始浓度为2 mol/L和4 mol/L的实验,测得反应消耗CCl4的百分率(x%)和生成物中CHCl3的百分含量(y%)随时间(t)的变化关系如图(图中实线是消耗CCl4的百分率变化曲线,虚线是产物中CHCl3的百分含量变化曲线)。

①在图中的四条线中,表示H2起始浓度为2 mol/L的实验消耗CCl4的百分率变化曲线是________(选填序号)。
②根据上图曲线,氢气的起始浓度为________ mol/L时,有利于提高CCl4的平衡转化率和产物中CHCl3的百分含量。你判断的依据是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.25 ℃时,1 L 0.1 mol·L-1的CH3COOH溶液中,含氢离子数约为0.1NA
B.标准状况下,22.4 L CHCl3中含氯原子数为3NA
C.1mol Na2O2晶体中所含离子数为3NA
D.0.5 mol NaCl晶体中含0.5NA个NaCl分子
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列给定条件的溶液中,一定大量共存的离子组是
A.1.0 mol·L-1的Na2CO3溶液:
Fe2+、H+、Cl-、SO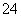
B.甲基橙呈红色的溶液:Na+、K+、SiO 、NO
、NO
C.由水电离出的c(H+)=2.0×10-10的溶液中:
Ba2+、K+、Cl-、HCO
D.含大量Al3+的溶液中:Cu2+、Na+、SO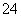 、NO
、NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com