
| A. | 一定条件下,乙酸乙酯、葡萄糖、蛋白质都能与水发生水解反应 | |
| B. | 乙二醇、丙氨酸均可发生缩聚反应 | |
| C. | 从海水中提取镁、溴、碘及从海水中生产烧碱、食盐、纯碱的过程中均涉及氧化还原反应 | |
| D. | 自然界中含有大量的游离态的硅,硅单质可用于制作计算机芯片 |
分析 A.葡萄糖不能发生水解;
B.含-OH或-COOH可发生缩聚反应;
C.从海水中提取镁盐,通常将熟石灰加入海水中或卤水中,沉淀出氢氧化镁,氢氧化镁与盐酸反应生成氯化镁,电解熔融状态的氯化镁,就能制的金属镁;海水提溴是先氧化溴离子为溴单质,再用还原剂还原溴单质为溴离子,再用氧化剂氧化溴离子为溴单质;从海带中提取单质碘:先将海带烧成灰,向灰中加水搅拌,再过滤得含碘离子的滤液,取滤液通入足量氯气,然后加入CCl4振荡,最后用分液漏斗分液;海水制备烧碱是饱和氯化钠电解生成,发生的是氧化还原反应,海水蒸发制海盐的过程中是利用氯化钠溶解度随温度变化不大,蒸发水得到氯化钠晶体,氨化的饱和食盐水中纳入二氧化碳生成碳酸氢钠和氯化铵,碳酸氢钠受热分解生成碳酸钠;
D.自然界中无游离态的硅.
解答 解:A.一定条件下,乙酸乙酯、蛋白质都能与水发生水解反应,葡萄糖为单糖,不能发生水解,故A错误;
B.含-OH或-COOH可发生缩聚反应,则乙二醇、丙氨酸均可发生缩聚反应,故B正确;
C.从海水中提取镁、溴、碘及从海水中生产烧碱的过程中均涉及氧化还原反应,食盐、纯碱不涉及氧化还原反应,故C错误;
D.硅单质可用于制作计算机芯片,自然界中不含有大量的游离态的硅,硅元素存在是氧化物和硅酸盐,故D错误;
故选B.
点评 本题考查了有机物性质、海水提取过程的分析理解、注意知识的积累,题目难度中等.


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:选择题

| A. | 电子从电极a经电解质溶液流向电极b | |
| B. | 电池放电时Na+从b极区移向a极区 | |
| C. | 放电一段时间后,正极消耗的OH-和负极生成的OH-的量相等 | |
| D. | 电池的负极反应为BH4--8e-+8OH-=BO2+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用燃烧法可鉴别羊毛制品和涤纶制品 | |
| B. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 | |
| C. | 二氧化硫可广泛用于食品的增白 | |
| D. | 次氯酸钠溶液可用于环境的消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
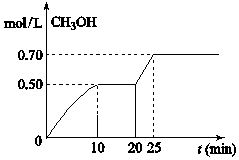 在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )
在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )| A. | 从开始到25分钟,CO2的转化率是35% | |
| B. | 从20分钟到25分钟,可能是缩小容器体积 | |
| C. | 其它条件不变,将温度升到800℃,平衡常数增大 | |
| D. | 从反应开始到10分钟,H2的平均反应速率v(H2)=0.15mol(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10:1 | B. | 1:10 | C. | 9:2 | D. | 2:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 久置的植物油发出难闻的气味是因为发生了氧化反应 | |
| B. | 《本草钢木》记载民间酿酒的工艺:“凡酸坏之酒,皆可蒸烧…”,这里用到的分离坏酒的方法在原理上是化学变化 | |
| C. | 硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果 | |
| D. | 在牙膏中添加Na2PO3F、NaF或SrF2等均能防治龋齿,当提供的F-浓度相同时,它们的作用是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com