
 Č”µČĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗĮ½·ŻAŗĶB£¬Ćæ·Ż10mL£¬·Ö±šĻņA”¢BÖŠĶØČė²»µČĮæµÄCO2£¬ŌŁ¼ĢŠųĻņĮ½ČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol/LµÄŃĪĖį£¬±ź×¼×“æöĻĀ²śÉśµÄCO2ĘųĢåĢå»żÓėĖł¼ÓµÄŃĪĖįČÜŅŗĢå»żÖ®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ŹŌ»Ų“š£ŗ
Č”µČĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗĮ½·ŻAŗĶB£¬Ćæ·Ż10mL£¬·Ö±šĻņA”¢BÖŠĶØČė²»µČĮæµÄCO2£¬ŌŁ¼ĢŠųĻņĮ½ČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol/LµÄŃĪĖį£¬±ź×¼×“æöĻĀ²śÉśµÄCO2ĘųĢåĢå»żÓėĖł¼ÓµÄŃĪĖįČÜŅŗĢå»żÖ®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ŹŌ»Ų“š£ŗ·ÖĪö £Ø1£©ĻČĻņĒāŃõ»ÆÄĘČÜŅŗÖŠĶØČė¶žŃõ»ÆĢ¼£¬ŗóĻņĶØČė¶žŃõ»ÆĢ¼µÄĒāŃõ»ÆÄĘČÜŅŗÖŠµĪ¼ÓŃĪĖį£¬µ±¶žŃõ»ÆĢ¼ĘųĢåĶźČ«·Å³öŹ±£¬ČÜŅŗµÄČÜÖŹŹĒĀČ»ÆÄĘ£¬øĆ·“Ó¦µÄŹµÖŹŹĒŃĪĖįŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĀČ»ÆÄĘ£¬øł¾ŻŃĪĖįµÄĪļÖŹµÄĮæ¼ĘĖćĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæÅØ¶Č£»
£Ø2£©µ±Éś³ÉCO2ĘųĢåŹ±£¬·¢Éś·“Ó¦HCO3-+H+=H2O+CO2”ü£¬¶ŌÓŚAČÜŅŗĄ“Ėµ£¬µĪ¼ÓŃĪĖį60mLŹ±Ć»ÓŠĘųĢåÉś³É£¬æÉÄÜ·¢ÉśOH-+H+=H2OŗĶCO32-+H+=HCO3-£¬øł¾ŻĻūŗÄŃĪĖįĢå»żĻą¶Ō“óŠ”Č·¶ØĖłµĆČÜŅŗÖŠµÄČÜÖŹ£»
£Ø3£©µ±Éś³ÉCO2ĘųĢåŹ±£¬·¢Éś·“Ó¦HCO3-+H+=H2O+CO2”ü£¬¶ŌÓŚBČÜŅŗĄ“Ėµ£¬µĪ¼ÓŃĪĖį25mLŹ±Ć»ÓŠĘųĢåÉś³É£¬æÉÄÜ·¢ÉśOH-+H+=H2OŗĶCO32-+H+=HCO3-£¬øł¾ŻĻūŗÄŃĪĖįĢå»żĻą¶Ō“óŠ”Č·¶ØĖłµĆČÜŅŗÖŠµÄČÜÖŹ£¬“Ó¶ųČ·¶Ø·¢ÉśµÄĄė×Ó·“Ó¦£»
£Ø4£©ĻČČ·¶ØBČÜŅŗÖŠµÄČÜÖŹ£¬ŌŁøł¾ŻĢ¼ĖįĒāÄĘŗĶŃĪĖįµÄ·“Ó¦·½³ĢŹ½¼ĘĖćÉś³É¶žŃõ»ÆĢ¼µÄĢå»ż£®
½ā“š ½ā£ŗ£Ø1£©¼ÓČė75mlŃĪĖįŹ±¶žŃõ»ÆĢ¼µÄĢå»ż“ļ×ī“󣬓ĖŹ±ČÜŅŗĪŖĀČ»ÆÄĘČÜŅŗ£®øł¾ŻĀČĄė×Ó”¢ÄĘĄė×ÓŹŲŗć£¬
ĖłŅŌn£ØNaOH£©=n£ØNaCl£©=n£ØHCl£©=0.075ml”Į0.1mol/L=0.0075mol£¬
ĖłŅŌc£ØNaOH£©=$\frac{0.0075mol}{0.01L}$=0.75mol/L£¬
¹Ź“š°øĪŖ£ŗ0.75mol/L£»
£Ø2£©CO2ÓėNaOH·“Ó¦ĪŖ¢ŁCO2+NaOH=NaHCO3£¬¢ŚCO2+2NaOH=Na2CO3+H2O£¬
µ±n£ØCO2£©£ŗn£ØNaOH£©”Ż1£¬·“Ó¦°“¢Ł½ųŠŠ£¬µČÓŚ1Ź±£¬CO2”¢NaOHĒ”ŗĆ·“Ӧɜ³ÉNaHCO3£»“óÓŚ1Ź±£¬Éś³ÉÉś³ÉNaHCO3£¬CO2ÓŠŹ£Óą£»
$\frac{1}{2}$£¼n£ØCO2£©£ŗn£ØNaOH£©£¼1£¬·“Ó¦°“¢Ł¢Ś½ųŠŠ£¬CO2”¢NaOH·“Ó¦£¬ĪŽŹ£Óą£¬Éś³ÉĪļĪŖNaHCO3”¢Na2CO3£»
µ±n£ØCO2£©£ŗn£ØNaOH£©”Ü$\frac{1}{2}$£¬·“Ó¦°“¢Ś½ųŠŠ£¬µČÓŚ$\frac{1}{2}$£¬Ź±£¬CO2”¢NaOHĒ”ŗĆ·“Ӧɜ³ÉNa2CO3£»Š”ÓŚ$\frac{1}{2}$Ź±£¬Éś³ÉNa2CO3£¬NaOHÓŠŹ£Óą£»
¹Ź“š°øĪŖ£ŗNa2CO3£¬NaOH£»
£Ø3£©µ±Éś³ÉCO2ĘųĢåŹ±£¬·¢Éś·“Ó¦HCO3-+H+=H2O+CO2”ü£¬¶ŌÓŚBČÜŅŗĄ“Ėµ£¬µĪ¼ÓŃĪĖį25mLŹ±Ć»ÓŠĘųĢåÉś³É£¬æÉÄÜ·¢ÉśOH-+H+=H2OŗĶCO32-+H+=HCO3-£¬¼ŁÉčŌČÜŅŗÖŠÖ»ÓŠĢ¼ĖįÄĘ£¬Éś³ÉĢ¼ĖįĒāÄĘŠčŅŖŃĪĖįµÄĢå»żŗĶĢ¼ĖįĒāÄĘÉś³ÉĀČ»ÆÄĘŠčŅŖŃĪĖįµÄĢå»żĻąµČ£¬Źµ¼ŹÉĻŠčŅŖŃĪĖįµÄĢå»żŠ”ÓŚĢ¼ĖįĒāÄĘÉś³ÉĀČ»ÆÄĘŠčŅŖŃĪĖįµÄĢå»ż£¬ĖµĆ÷ŌČÜŅŗÖŠµÄČÜÖŹŹĒĢ¼ĖįÄĘŗĶĢ¼ĖįĒāÄĘ£¬ĖłŅŌBĻßÖŠĻūŗÄŃĪĖį0£¼v£ØHCl£©£¼25mLŹ±·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ£ŗH++CO32-=HCO3-£¬
¹Ź“š°øĪŖ£ŗH++CO32-=HCO3-£»
£Ø4£©ÓÉĒśĻßBæÉÖŖ“Ó25mlµ½75mlĪŖĢ¼ĖįĒāÄĘÓėŃĪĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼£¬·“Ó¦·½³ĢŹ½ĪŖNaHCO3+HCl=NaCl+CO2”ü+H2O£¬
ĖłŅŌn£ØCO2£©=n£ØHCl£©=£Ø0.075ml-0.025ml£©”Į0.1mol/L=0.005mol£¬
ĖłŅŌCO2ĘųĢåĢå»żĪŖ0.005mol”Į22.4L/mol=0.112L=112mL£¬
¹Ź“š°øĪŖ£ŗ112£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļµÄÓŠ¹Ų¼ĘĖć£¬ÄѶČÖŠµČ£¬¹Ų¼üøł¾ŻĶ¼ÖŠŃĪĖįµÄĢå»ż¼ĘĖć³öNaOH”¢CO2µÄĪļÖŹµÄĮ棬Ŋ¶ĻCO2ÓėNaOH·“Ó¦¹ż³Ģ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH=7µÄČÜŅŗ | |
| B£® | c£ØH+£©=10-6mol/L“æĖ® | |
| C£® | Ź¹ŹÆČļŹŌŅŗ³Ź×ĻÉ«µÄČÜŅŗ | |
| D£® | ĖįÓė¼īĒ”ŗĆĶźČ«·“Ӧɜ³ÉÕżŃĪµÄČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4LC2H2”¢C2H6µÄ»ģŗĻĘųĢåÓė22.4LC2H4ÖŠĖłŗ¬Ō×Ó×ÜŹż¾łĪŖ6NA | |
| B£® | ³£ĪĀĻĀ£¬1L PH=14µÄNaOHČÜŅŗÖŠÓÉĖ®µēĄė³öµÄOH-øöŹżĪŖNA | |
| C£® | ±ź×¼×“æöĻĀ£¬11.2LµÄ12C16OŗĶ14N2µÄ»ģŗĻĘųĢåÖŠĖłŗ¬ÖŠ×ÓŹżŗĶŌ×ÓŹżµÄ²īÖµĪŖ6NA | |
| D£® | ½«200mL0.1mol•L-1FeCl3ČÜŅŗÖĘ³É½ŗĢ壬ĖłµĆFe£ØOH£©3½ŗĢåĮ£×ÓŹżĪŖ0.02NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaHSO4ČÜŅŗÓėBa£ØOH£©2ČÜŅŗ·“Ó¦ÖĮÖŠŠŌ£ŗH++SO42-+Ba2++OH-ØTBaSO4”ż+H2O | |
| B£® | Mg£ØOH£©2ÓėH2SO4·“Ó¦£ŗMg2++2OH-+2H++SO42-ØTMgSO4”ż+2H2O | |
| C£® | Ć¾Óė“×Ėį·“Ó¦””Mg+2H+ØTMg2++H2”ü | |
| D£® | Na2SO3ČÜŅŗŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£ŗ5SO32-+6H++2MnO4-ØT5SO42-+2Mn2++3H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
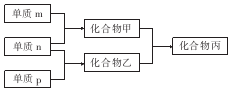 ¶ĢÖÜĘŚÖ÷×åŌŖĖŲX”¢Y”¢ZµÄµ„ÖŹm”¢n”¢pŌŚĶس£×“æöĻĀ¾łĪŖĘųĢ¬£¬²¢ÓŠĻĀĮŠ×Ŗ»Æ¹ŲĻµ£Ø·“Ó¦Ģõ¼žĀŌČ„£©£ŗĘäÖŠĖ«Ō×Óµ„ÖŹ·Ö×ÓÖŠ£¬µ„ÖŹmŗ¬¹²ÓƵē×Ó¶ŌŹż×ī¶ą£¬¼×ŗ¬ÓŠ10µē×Ó£¬ŅŅŗ¬ÓŠ18µē×Ó£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
¶ĢÖÜĘŚÖ÷×åŌŖĖŲX”¢Y”¢ZµÄµ„ÖŹm”¢n”¢pŌŚĶس£×“æöĻĀ¾łĪŖĘųĢ¬£¬²¢ÓŠĻĀĮŠ×Ŗ»Æ¹ŲĻµ£Ø·“Ó¦Ģõ¼žĀŌČ„£©£ŗĘäÖŠĖ«Ō×Óµ„ÖŹ·Ö×ÓÖŠ£¬µ„ÖŹmŗ¬¹²ÓƵē×Ó¶ŌŹż×ī¶ą£¬¼×ŗ¬ÓŠ10µē×Ó£¬ŅŅŗ¬ÓŠ18µē×Ó£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | XŹĒĶ¬ÖÜĘŚÖŠ·Ē½šŹōŠŌ×īĒæµÄŌŖĖŲ | |
| B£® | ŌŖĖŲX”¢Y”¢ZµÄŌ×Ó°ė¾¶“󊔹ŲĻµĪŖX£¼Y£¼Z | |
| C£® | ZµÄŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌŌŚÖ÷×åŌŖĖŲÖŠ×īĒæ | |
| D£® | »ÆŗĻĪļ±ūŹĒĄė×Ó»ÆŗĻĪļ£¬¼Čŗ¬Ąė×Ó¼üÓÖŗ¬¹²¼Ū¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
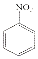 $”ś_{HCl}^{Fe}$
$”ś_{HCl}^{Fe}$
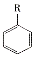 £ØR-Ķ黳£©$\stackrel{KMnO_{4}/H+}{”ś}$
£ØR-Ķ黳£©$\stackrel{KMnO_{4}/H+}{”ś}$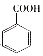
 +2NaOH$”ś_{”÷}^{H_{2}O}$
+2NaOH$”ś_{”÷}^{H_{2}O}$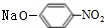 +NaCl+H2O£®
+NaCl+H2O£®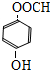 £®
£®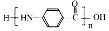 µÄŗĻ³ÉĀ·Ļß
µÄŗĻ³ÉĀ·Ļß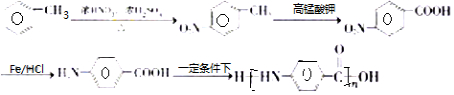 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6ÖÖ | B£® | 9ÖÖ | C£® | 10 ÖÖ | D£® | 12 ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
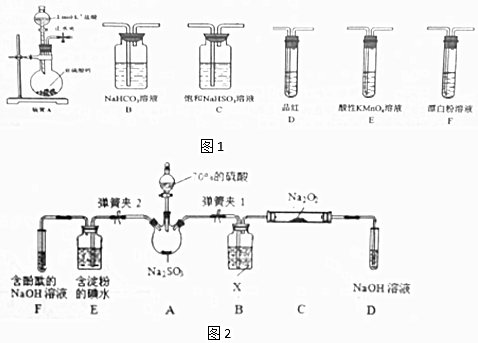
| ²Ł×÷²½Öč | ŹµŃéĻÖĻó | ½āŹĶŌŅņ |
| ¹Ų±ÕµÆ»É¼Š2£¬“ņæŖµÆ»É¼Š1£¬×¢ČėĮņĖįÖĮ½žĆ»Čż¾±ÉÕĘæÖŠ¹ĢĢå | Čō½«“ų»šŠĒµÄľĢõ·ÅŌŚDŹŌ¹ÜæŚ“¦£¬Ä¾Ģõ²»ø“Č¼ | SO2ÓėNa2O2·“Ó¦ĪŽO2Éś³É£¬æÉÄÜ·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ¢ŁNa2O2+SO2=Na2SO4 |
| Čō½«“ų»šŠĒµÄľĢõ·ÅŌŚDŹŌ¹ÜæŚ“¦£¬Ä¾Ģõø“Č¼ | SO2ÓėNa2O2·“Ó¦ÓŠO2Éś³É£¬·¢ÉśµÄ»Æѧ·“Ó¦ĪŖ£ŗ2SO2+2Na2O2ØT2Na2SO3+O2 | |
| ¹Ų±ÕµÆ»É¼Š1£¬“ņæŖµÆ»É¼Š2£¬²ŠÓąĘųĢå½ųČėE£¬FÖŠ£® | EÖŠ¢ŚE ÖŠČÜŅŗĄ¶É«ĶŹČ„ | EÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½¢ŪSO2+I2+2H2O=2I-+SO42-+4H+ |
| FÖŠ¢ÜF ÖŠŗģÉ«±äĒ³»ņĶŹÉ« | FÖŠ·“Ó¦ĪŖ2OH-+SO2ØTSO32-+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ„Š±Įņ×Ŗ»ÆĪŖÕż½»ĮņŠčŅŖĪüČČ | B£® | µ„Š±Įņ±ČÕż½»ĮņĪČ¶Ø | ||
| C£® | ”÷H4£¾”÷H5 | D£® | ”÷H4£¼0 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com