
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 颜色、性质 | 物质 | 颜色、性质 |
| 氢氧化铜Cu(OH)2 | 蓝色固体不溶于水 | 硫酸铜(CuSO4) | 溶液呈蓝色 |
| 氧化亚铜(CuO) | 红色固体不溶于水 | 氯化铜(CuCl2) | 溶液呈绿色,稀溶液呈蓝色 |
| 氯化亚铜(CuCl) | 白色固体不溶于水 | 碱式氯化铜 | 绿色固体不溶于水 |
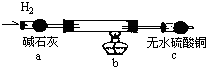
查看答案和解析>>
科目:高中化学 来源:2012届江苏省重点中学高三下学期开学质量检测化学试卷 题型:实验题
(16分)某兴趣小组,对物质A的组成和性质,进行了如下系列研究:
实验1:对A的溶液进行了焰色反应;现象:火焰呈绿色。
实验2:从A的溶液中获取固体A。
实验3:加热干燥的固体A9.4g,出现大量的红棕色气体,经处理集得不溶于水的气体0.56L(标况下),且该气体能使带火星的木条复燃,残留黑色固体4.0g。
实验4:用酒精喷灯再对黑色固体加热,待固体完全 变红,又集得能使带火星的木条复燃的气体0.28L(标况下)。
变红,又集得能使带火星的木条复燃的气体0.28L(标况下)。
资料:①氧化亚铜属碱性氧化物,在酸性介质中能发生自身氧化还原反应;在空气中灼烧会转化为黑色固体,而在高温下较为稳定。
②酒精灯的火焰温度一般在400-500℃;酒精喷灯的火焰温度一般在1000℃左右;
根据题中信息,回答下列问题:
(1)实验1中进行焰色反应实验时,一次完整的操作次序为 (填序号,可重复);
a.灼烧 b.用盐酸清洗铂丝 c. 用铂丝蘸取待测液
(2)实验2中如何从溶液中获取固体A? ;
实验中所需主要的仪器有:铁架台(附铁圈)、 ;
(3)实验3中经处理集得不溶于水的气体0.56L,这里的“经处理”是将气体通过 ,然后用排水法收集气体。
(4)写出实验3中的分解反应式: ;
(5)写出实验4中的分解反应式: ;
(6)实验4中红色固体为纯净物,化学式可以通过计算来确定,也可以通过实验来进一步确定,请设计一个简单的实验确定方案,并写出所发生的反应式。 。
查看答案和解析>>
科目:高中化学 来源:2014届山西省高一2月月考化学试卷 题型:实验题
(共13分)(1)右图甲中装置甲是某种不溶于水的气体X的发生装置和收集装置(必要时可以加热),所用的试剂从下列试剂中选取2-3种:硫化亚铁、二氧化锰、铜屑、氯化铵、稀氨水、大理石、浓硫酸、浓硝酸、稀硝酸、蒸馏水。
回答下列问题:
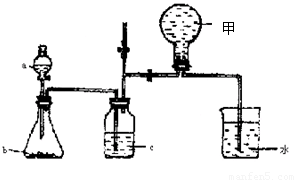
①气体X的分子式是 。
②所选择的药品a是 ,b是 , c是 。
③下列装置乙和丙,能代替装置甲的简易装置是 (填“乙”或“丙”)
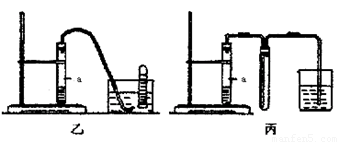
④请写出在试管a中所发生反应的化学方程式 。
⑤从反应开始到反应结束,预期在试管a中可观察到的气体的实验现象有哪些,请依次逐步写出 ; ;
(2)在进行研究性学习的过程中,学生发现等质量的铜片分别与等质量均过量的浓硝酸或稀硝酸反应,所得到溶液前者呈绿色,后者呈蓝色,针对这种现象,学生进行了讨论,出现两种意见,一种认为:Cu2+浓度差异引起了这种现象,你认为 (填“正确”或“不正确”),依据是: ;
另一种意见是:溶液呈绿色可能是Cu2+与NO2混合的结果,并用实验进行了证明,请简述实验方案与实验现象: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com