
| A. | HA较强 | B. | HB较强 | C. | 两者一样 | D. | 无法比较 |
分析 根据强酸制取弱酸知,等物质的量浓度的两种弱酸的钠盐(NaA、NaB)溶液中分别通入适量的CO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3,说明HA的酸性小于碳酸而大于碳酸氢根离子,2NaB+CO2+H2O=2HB+Na2CO3,说明HB的酸性小于碳酸氢根离子,据此分析.
解答 解:等物质的量浓度的两种弱酸的钠盐(NaA、NaB)溶液中分别通入适量的CO2,
发生如下反应:NaA+CO2+H2O=HA+NaHCO3,说明HA的酸性小于碳酸而大于碳酸氢根离子,即酸性:H2CO3>HB>HCO3 -,
2NaB+CO2+H2O=2HB+Na2CO3,说明HB的酸性小于碳酸氢根离子,即酸性:HCO3 ->HB,
综上可知酸性:H2CO3>HA>HCO3 ->HB,所以HA较强,
故选A.
点评 本题考查了酸性强弱的判断,明确强酸制取弱酸的原理是解本题关键,题目难度不大,侧重于考查学生对基本原理的应用能力.


科目:高中化学 来源: 题型:解答题
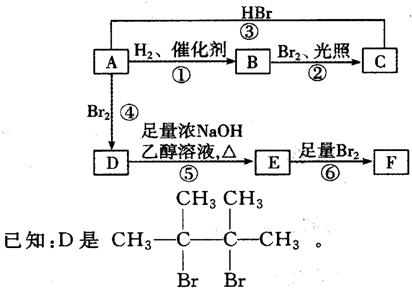
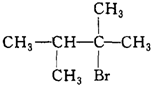 .
. ;;写出由E-F的化学方程式
;;写出由E-F的化学方程式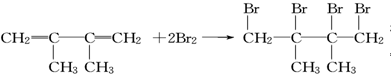 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
.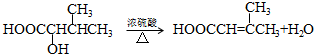 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇含有的分子数为 NA | |
| B. | 1.8g的NH4+离子中含有的电子数为NA | |
| C. | 在含1mol氢氧化铁的胶体中,胶粒数目为NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
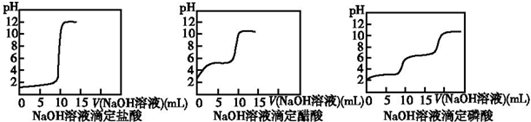
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{ab}{22400}$mol•L-1 | B. | $\frac{ab}{22400+17a}$mol•L-1 | ||
| C. | $\frac{1000ab}{22400+35a}$mol•L-1 | D. | $\frac{1000ab}{22400+17a}$mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 比较金属性:Mg>Al | 往盛同浓度同体积的盐酸的两试管中分别加入Mg条和Al粉 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2mL 1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
| C | 比较氧化性:Fe3+>I- | 往滴有CCl4的FeI2溶液中慢慢滴加氯水 |
| D | 配制1.0mol/L的NaOH溶液 | 称取4g NaOH晶体溶于100mL蒸馏水中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
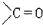 +RMgX→
+RMgX→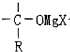 $\stackrel{H_{2}O}{→}$
$\stackrel{H_{2}O}{→}$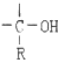
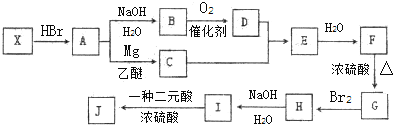
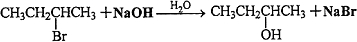 ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
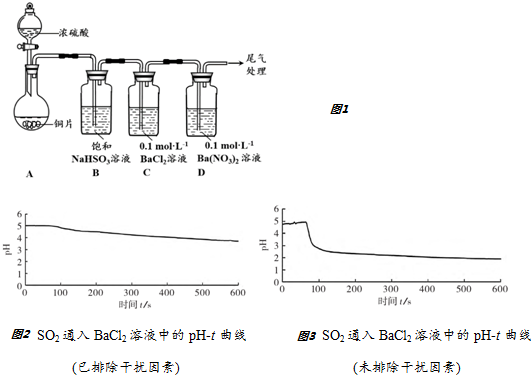
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com