
����Ŀ����ҵ�������е�һ����Ҫ��Ӧ��SO2��400��500 ���µĴ�������2SO2��O2![]() 2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д������( )
2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д������( )
A. ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч��
B. �����������£�SO2������100%��ת��ΪSO3
C. Ϊ�����SO2��ת���ʣ�Ӧ�ʵ����O2��Ũ��
D. �ﵽƽ��ʱ��SO2��Ũ����SO3��Ũ�����
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У�����ȷ����
A.��֬ˮ��IJ����к�����
B.���ϡ��ϳ���֬�ͺϳ�����Ϊ������ϳɲ�����
C.�����ʿ�ˮ�����ɶ��ĺͰ�����
D.ҽ������ 75%�ľƾ���������Ϊ����ʹ�����ʱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������淶���ܴﵽĿ�ĵ���
Ŀ�� | ���� | |
A�� | ȡ20.00 mL���� | ��50 mL��ʽ�ζ�����װ�����ᣬ������ʼ����Ϊ30.00mL��ʣ�����������ƿ |
B�� | ��ϴ������ʵ�������Թ� | ���þƾ���ϴ������ˮ��ϴ |
C�� | �ⶨ��������ҺpH | �ò�����պȡ��Һ������ʪ���pH��ֽ�� |
D�� | ����Ũ��Ϊ0.010 | ��ȡKMnO4����0.158 g������100 mL����ƿ�У���ˮ�ܽⲢϡ�����̶� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NiSO4������ˮ����ˮ��Һ�����ԣ��ж�����Ҫ���ڵ�ƹ�ҵ��Ҳ�ǽ��������ӵ���Դ��NiSO4��6H2O��һ����ɫ������ˮ�ľ��壬���ɵ�Ʒ����������⣬������ͭ��п������Ԫ�أ�Ϊԭ�ϻ�ã������������£�

��1��NiSO4ˮ��Һ������ԭ����_________________________��
��2������Һ���м���H2O2�����ӷ���ʽ��_________________________��
��3������Һ��pH��Ŀ���dz�ȥFe3+��ԭ����Fe3++3H2O![]() Fe��OH��3+3H+����֪25��ʱKsp[Fe��OH��3]=2.8��10��39������¶���������Ӧ��ƽ�ⳣ��K=______�����ʵ��֤��Fe3+�ѳ���_________________��
Fe��OH��3+3H+����֪25��ʱKsp[Fe��OH��3]=2.8��10��39������¶���������Ӧ��ƽ�ⳣ��K=______�����ʵ��֤��Fe3+�ѳ���_________________��
��4����Һ�����ʵ���Ҫ�ɷ���NiSO4����Na2CO3���˺�õ�NiCO3���壬�ټ�����ϡ�����ܽ�������NiSO4��������������Ŀ����______��
��5����d(NiSO4��Һ)��______��______��______ϴ�ӡ�����Ȳ����ɵõ�NiSO4��6H2O���壻
��6��Ϊ����߲��ʣ�����õ�NiSO4��6H2O��ʣ��Һ��Ҫѭ��ʹ�ã���Ӧ�û����������е�______λ�ã���a��b��c��d����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
������G��һ�ֿ���������������ҩ�ʵ�����ɷ�����A�Ʊ�G�ĺϳ�·�����£�

�ش��������⣺
��1��A�Ľṹ��ʽΪ____________��C�Ļ�ѧ������______________��
��2���۵ķ�Ӧ�Լ��ͷ�Ӧ�����ֱ���____________________���÷�Ӧ��������__________��
��3���ݵķ�Ӧ����ʽΪ_______________�������һ���л����������____________��
��4��G�ķ���ʽΪ______________��
��5��H��G��ͬ���칹�壬�䱽���ϵ�ȡ������G����ͬ��λ�ò�ͬ����H���ܵĽṹ��______�֡�
��6��4-����������������![]() ������Ҫ�ľ�ϸ�����м��壬д���ɱ����ѣ�
������Ҫ�ľ�ϸ�����м��壬д���ɱ����ѣ�![]() ���Ʊ�4-���������������ĺϳ�·��___________�������Լ���ѡ����
���Ʊ�4-���������������ĺϳ�·��___________�������Լ���ѡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ�����������գ�
��1��1 mol NaHSO4����ˮ�ܵ����___________________��SO42����
��2��1.7![]()
![]() ��
��![]() ԭ�����ʵ���Ϊ_____________��������Ϊ______����֪
ԭ�����ʵ���Ϊ_____________��������Ϊ______����֪![]()
![]() ��ԭ����Ϊ
��ԭ����Ϊ![]() ����٤������Ϊ______���ú�
����٤������Ϊ______���ú�![]() ��
��![]() �Ĵ���ʽ��ʾ����
�Ĵ���ʽ��ʾ����
��3������£�����������������������֮��Ϊ __________________����ԭ�Ӹ���֮�� _______________��
��4��ij�����Ȼ���MClx��Ħ������Ϊ133.5g/mol��ȡ�ý����Ȼ���26.7g���ˮ��Һ��������AgNO3��Һ��ȫ��Ӧ������86.1g��ɫ�����������M��Ħ������Ϊ _______________________��
��5����״���£��ܶ�Ϊ0.75g/L��NH3��CH4��ɵĻ�������У�NH3���������Ϊ______���û�����������������ܶ�Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016�궬��ȫ���ֵ�������������������β�������������ԭ��֮һ������β����CO��NO���ж����塣Ϊ�˼���CO�Դ�������Ⱦ��ij�о���ѧϰС�����о�CO��H2O��Ӧת��Ϊ��ɫ��ԴH2����֪��
2CO(g)+O2(g)��2CO2(g)�� ��H = ��566kJ��moL��1
2H2(g)+O2(g)��2H2O(g)�� ��H = ��483.6KJ��moL��1
H2O (g)��H2O(l)�� ��H = ��44.0KJ��moL��1
��1������ȼ���Ȧ�H=__________��
��2��д��CO��H2O(g)��������CO2��H2���Ȼ�ѧ����ʽ______________��
��3����1L�������������м���0.200mol CO��1.00mol H2O(g)����t��ʱ��Ӧ���ﵽƽ�⣬���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=1������ʽ�и�����ǰ��ѧ������Ϊ��������ȣ�����t��ʱCO��ת����Ϊ________����Ӧ�ﵽƽ��������¶ȣ���ʱƽ�ⳣ����____�����������䡱��С������
��4��������β���з����CO��O2��������Na2CO3��ɵ�ȼ�ϵ�أ�ͬʱ���õ�ⷨ�Ʊ�N2O5��װ����ͼ��ʾ������YΪCO2��д��ʯīI�缫�Ϸ�����Ӧ�ĵ缫��Ӧʽ_______________________________���ڵ���������N2O5�ĵ缫��ӦʽΪ__________________________________��

��5����һ�������£���NH3��������β���е�NO����֪NO��NH3������Ӧ����N2��H2O������NO��NH3�Ļ����1mol����ַ�Ӧ��õ��Ļ�ԭ��������������1.4 g����ԭ��Ӧ�������NO�����ʵ���������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Խ�������ת����
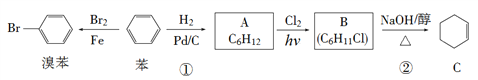
�ش��������⣺
��1����Ӧ�ٵķ�Ӧ����Ϊ________��������A�Ļ�ѧ����Ϊ___________��
��2��������B�Ľṹ��ʽΪ_________����Ӧ�ڵķ�Ӧ����Ϊ_______��
��3����ν���ˮ���𱽺��屽__________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com