
【题目】实验室中要测定部分变质的过氧化钠的纯度,可用如图装置实现。
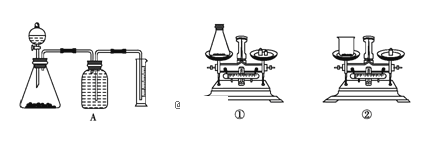
(1)锥形瓶中应放______,分液漏斗中放______,锥形瓶中发生反应的化学方程式为_______________________________。
(2)如图用托盘天平称取样品,应选用如图中的____(填“①”或“②”)。不选用另一装置的原因是_________________________________________________________。
(3)若取用样品的质量为2.5 g,收集到气体的体积为280 mL(标准状况),计算样品中Na2O2的质量分数__(写出计算过程)。
【答案】Na2O2样品H2O2Na2O2+2H2O4NaOH+O2↑①过氧化钠容易吸收空气中的H2O和CO2,不宜暴露在空气中称量78%
【解析】
(1)Na2O2和空气中二氧化碳反应生成Na2CO3,Na2CO3易溶于水但和水不反应,Na2O2和水反应生成NaOH和氧气,所以锥形瓶中应盛Na2O2,分液漏斗中装水;
(2)用托盘天平称量药品时应该遵循“左物右砝”原则,过氧化钠易和空气中水、二氧化碳反应,应该密封称量;
(3)只有Na2O2和水反应生成O2,根据氧气和Na2O2之间的关系式计算Na2O2质量,从而计算其纯度。
(1)Na2O2和空气中二氧化碳反应生成Na2CO3,Na2CO3易溶于水但和水不反应,Na2O2和水反应生成NaOH和氧气,所以锥形瓶中应盛Na2O2,分液漏斗中装水,反应方程式为Na2O2+2H2O=4NaOH+O2↑,故答案为:Na2O2;水;Na2O2+2H2O=4NaOH+O2↑;
(2)用托盘天平称量药品时应该遵循“左物右砝”原则,过氧化钠易和空气中水、二氧化碳反应,应该密封称量,所以选①;不选用另一装置的原因是过氧化钠容易吸收空气中的H2O和CO2,不宜暴露在空气中称量;
(3)产生O2的物质的量为![]() =0.0125 mol,设过氧化钠的质量为m,
=0.0125 mol,设过氧化钠的质量为m,
2 Na2O2+2H2O=4NaOH+O2↑
2×78g 1 mol
m 0.0125mol
156g:1mol=m:0.0125mol,m=![]() =1.95g,样品中Na2O2的纯度为
=1.95g,样品中Na2O2的纯度为![]() ×100%=78%。
×100%=78%。


科目:高中化学 来源: 题型:
【题目】向猪膀胱内注入一半质量分数为30%的蔗糖溶液,扎紧入口,然后将其浸入质量分数为5%的蔗糖溶液中,每隔10 min称一次猪膀胱的重量,能正确表示测定结果的是下图中的
A.  B.
B. 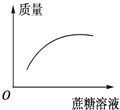
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,世界上多采用电解熔融氯化钠的方法来生产金属钠:2NaCl(熔融)![]() 2Na+Cl2↑。已知物质A、B、C、D、E、F有如图所示转化关系:
2Na+Cl2↑。已知物质A、B、C、D、E、F有如图所示转化关系:

请按要求书写:
(1)A→C的化学方程式:_______________________________________________________。
(2)B→D的化学方程式:___________________________________________________________。
(3)E+F→NaCl的化学方程式:____________________________________________。
(4)过氧化钠可用作制氧剂,写出过氧化钠与二氧化碳反应的化学方程式:______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知C2H6O存在两种结构C2H5OH和CH3OCH3。分子式为C5H12O且不能和金属钠反应放出氢气的有机物有(不考虑立体异构)( )
A. 5种 B. 6种
C. 7种 D. 8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从科学的角度来看,下列说法正确的是( )
A.冬天用煤炉取暖,为防止热量散失,应关紧门窗
B.进入古井前,应先做灯火试验
C.一次性塑料袋使用方便又经济,应大力提倡生产
D.油锅不慎着火,应立即用大量的水冲灭
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有N元素的化合物,下列关于判断错误的是( )
A.HNO3具有氧化性
B.NH3既具有氧化性又具有还原性
C.N2只具有还原性
D.NO2既具有氧化性又具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol;
(2)该气体所含原子总数为____________个;
(3)该气体在标准状况下的体积为____________L;
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为_____________;
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为____________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迄今距门捷列夫提出元素周期表已经151年。根据元素周期表和元素周期律,判断下列叙述不合理的是
A.位于第五周期的元素中主族序数大于周期数的元素为非金属元素
B.第35号元素的单质在常温常压下是液体
C.周期表中元素种类最多的一个族是第Ⅷ族
D.锗元素位于元素周期表中金属与非金属交界线附近
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com