
| A.定容时俯视液面 | B.配制时容量瓶没有干燥 |
| C.转移时没有洗涤烧杯和玻璃棒 | D.称量时砝码位置放错 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.铜和稀硝酸反应,排水法收集NO | B.锌和稀硝酸反应制氢气 |
| C.氮气和氧气反应制NO | D.加热氯化铵制取氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
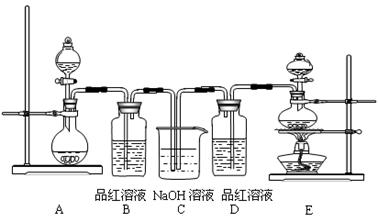
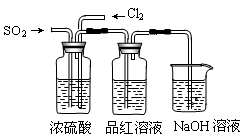
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
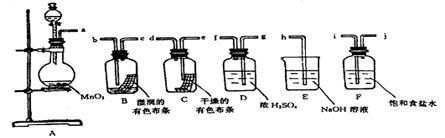
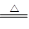 MnCl2 + Cl2↑+ 2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
MnCl2 + Cl2↑+ 2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。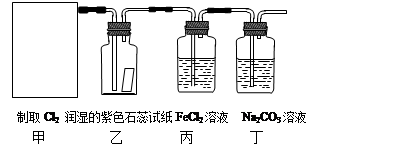
查看答案和解析>>
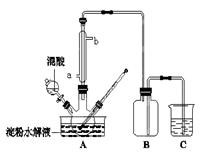
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.观察酸式滴定管液面时,开始俯视,滴定终点平视,所测出的碱液的浓度值 |
| B.用标准盐酸滴定未知浓度的氢氧化钠溶液时,酸式滴定管洗净后,没有用标准盐酸润洗而直接装标准盐酸滴定碱液,所测出的碱液的浓度值 |
| C.用已知浓度的盐酸溶液滴定未知浓度的氢氧化钠溶液用酚酞做指示剂所测出的碱液的浓度值 |
| D.做中和热测定时,在大小两个烧杯之间没有垫碎泡沫塑料(或纸条)所测出的中和热数值 |
查看答案和解析>>
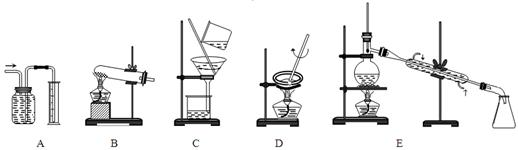
科目:高中化学 来源:不详 题型:实验题
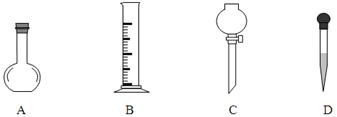
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com