
| A. | 一般来说,金属越活泼,越易发生腐蚀 | |
| B. | 金属发生腐蚀时表现了明显的氧化性 | |
| C. | 气温越高,金属越易腐蚀 | |
| D. | 金属腐蚀通常分化学腐蚀和电化学腐蚀两类 |
分析 A.金属越活泼,越易失电子;
B.金属发生腐蚀时金属原子失电子;
C.温度越高,反应速率越大;
D.金属和其它物质之间直接发生化学反应的属于化学腐蚀,含有杂质的金属在一定条件下能形成原电池,金属失电子被腐蚀.
解答 解:A.金属越活泼,越易失电子,则金属越活泼,越易发生腐蚀,故A正确;
B.金属发生腐蚀时金属原子失电子,所以金属发生腐蚀时表现了明显的还原性,故B错误;
C.温度越高,反应速率越大,所以气温越高,金属越易腐蚀,故C正确;
D.金属和其它物质之间直接发生化学反应的属于化学腐蚀,含有杂质的金属在一定条件下能形成原电池,金属失电子被腐蚀,所以金属腐蚀通常分化学腐蚀和电化学腐蚀两类,故D正确.
故选B.
点评 本题考查了金属的腐蚀,明确金属腐蚀的原因即可解答,难度不大,侧重于基础知识的考查.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氢氧化钡溶液与盐酸反应:OH-+H+=H2O | |
| B. | 向 FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl- | |
| C. | 小苏打溶液与烧碱溶液反应:HCO3-+OH-=CO32-+H2O | |
| D. | 氯气通入冷水中:Cl2+H2O=Cl-+ClO-+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称量8.75g食盐 | |
| B. | 用500ml的容量瓶配制480ml溶液 | |
| C. | 用10ml量筒量取6.46ml盐酸 | |
| D. | 用广泛pH试纸测得某溶液的pH为4.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2CaO+2S=2CaS+O2↑ | B. | S+O2=SO2 | ||
| C. | CaO+SO2=CaSO3 | D. | 2CaSO3+O2=2CaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
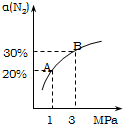 某温度下,对于反应N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A. | 将1.0mol氮气、3.0mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4kJ | |
| B. | 平衡状态由A变到B时,平衡常数K(A)<K(B) | |
| C. | 上述反应在达到平衡后,增大压强,H2的转化率提高 | |
| D. | 保持压强不变,通入惰性气体,平衡常数不变,平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com