
����Ŀ����֪ij��84����Һ��ƿ�岿�ֱ�ǩ��ͼ��ʾ������84����Һ��ͨ��ϡ��100��(���֮��)��ʹ�á���ش��������⣺
84����Һ
����Ч�ɷ֣�NaClO
�����1000ml
������������37.25%
���ܶȣ�1.2g.cm-3
(1)����84����Һ�������ʵ���Ũ��ԼΪ________mol��L-1������2λ��Ч���֣���
(2)ijͬѧȡ100 mL����84����Һ����ϡ�ͺ�����������ϡ�ͺ����Һ��c(Na��)_____mol��L-1(����С�����2λ)��
(3)��ͬѧ���ĸ���84����Һ�����䷽������NaClO��������230 mL��NaClO��������Ϊ37.25%������Һ��
����Ҫ����NaClO���������Ϊ___________g
�����������ɷֽ�Ϊ���¼�����
A.������ȷ��NaClO���壬�����ձ������������ˮʹ���ܽ⣬���ò���������
B.��Լ30mL����ˮ������ϴ���ձ��Ͳ���������ÿ�ε�ϴҺ����������ƿ��
C.��NaClO��ҺС�ĵ��ò�������������ƿ��D�����250mL����ƿ���Ƿ�©ˮ
E.������ˮֱ�Ӽ�������ƿ����Һ��ӽ��̶���
F.�ǽ�ƿ���������ߵ���ҡ����Һ
G.�ý�ͷ�ι�������ƿ����μ�������ˮ����Һ����͵�ǡ�����������
������������еĿհ״�_____________________����ȷ�IJ���˳����(����ĸ��д)��_______________������A�������ʱ������__________���ܽ��к���IJ�����
(4)��84����Һ����ϡ������ʹ�ÿ���������������ij����С����Ա��98%(�ܶ�Ϊ1.84g/ml)��Ũ��������100ml4.6mol/L��ϡ���ᣬ������ǿ��84����Һ��������������
�������Ƶ�ϡ�����У�H+�����ʵ���Ũ��Ϊ__________mol/L��
����Ҫ��ȡŨ��������Ϊ__________ml��
(5)�������Ƶ�ϡH2SO4���вⶨ������ʵ��Ũ��С��4.6 mol��L-1���������������Щ��������������Ũ��ƫС_______(����ĸ)��
A.����Ͳ��ȡŨ����ʱ��������Ͳ�Ŀ̶�
B.����ƿδ���T����������Һ
C.Ũ�������ձ���ϡ�ͺ�δ��ȴ������ת�Ƶ�����ƿ�У������ж���
D.������ƿת��ʱ��������Һ�彦��
E.ϴ����Ͳ�е�Һ��ע���ձ�
F.�ձ�δ����ϴ��
G.���ݺ�����ƿ������ҡ�ȣ����ú�Һ�治���̶��ߣ��ټ�ˮ���̶���
���𰸡�6.0 0.06 111.8 1-2cm�� DACBEGF ���ձ�����Һ��ȴ������ 9.2 25.0 DFG
��������
(1)����c=![]() �����㣻
�����㣻
(2)����ϡ��ǰ�����ʵ����ʵ������������㣻
(3)��ѡ����ʵ�������������Һ�����Ƽ�c=![]() ��m=n��M��������
��m=n��M��������
�ڸ���������Һ�IJ�����д�հ״���������֪��������
(4)�ٸ���c(H+)=2c(H2SO4)����c(H+)���㣻
�ڸ�����Һϡ��ǰ�����ʵ����ʵ���������㣻
(5)����c=![]() ���������������ʵ����ʵ��������Һ�������Ӱ���жϡ�
���������������ʵ����ʵ��������Һ�������Ӱ���жϡ�
(1)����84����Һ�������ʵ���Ũ��c(NaClO)=![]() mol/L=6.0mol/L��
mol/L=6.0mol/L��
(2)ϡ�ͺ�c(NaClO)=![]() c(NaClO)=
c(NaClO)=![]() ��6.0mol/L=0.06mol/L����ϡ�ͺ���Һ��Na+�����ʵ���Ũ��c(Na+)= c(NaClO)=0.06mol/L��
��6.0mol/L=0.06mol/L����ϡ�ͺ���Һ��Na+�����ʵ���Ũ��c(Na+)= c(NaClO)=0.06mol/L��
(3)��ʵ����û�й����230mL������ƿ������ѡ�������ı��������ԭ��Ҫѡ��ʹ��250mL������ƿ�������c=![]() ��֪��NaClO�����ʵ���n(NaClO)=c��V=6.0mol/L��0.25L=1.5mol����������m(NaClO)=1.5mol��74.5g/mol=111.8g��
��֪��NaClO�����ʵ���n(NaClO)=c��V=6.0mol/L��0.25L=1.5mol����������m(NaClO)=1.5mol��74.5g/mol=111.8g��
������һ�������һ�����ʵ���Ũ�ȵ���Һ������Ϊ���㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȡ�װƿ����ǩ������������E�У�������ˮֱ�Ӽ�������ƿ����Һ��ӽ��̶���1-2cm�������ý�ͷ�ιܵμ�����ˮ��
��ȷ�IJ���˳����D��A��C��B��E��G��F��
����ƿ������ҺҪ���¶�Ϊ���£������ܽ�һ�㶼�з��Ȼ������������Խ���A�������ʱ�����뽫�ձ�����Һ��ȴ�����£��ſ���ת����Һ��
(4)��c(H+)=2c(H2SO4)=2��4.6mol/L=9.2mol/L��
����Һϡ��ǰ�����ʵ����ʵ������䣬Ũ�����Ũ��Ϊc=![]() =18.4mol/L��������ҪŨ��������ΪV����V��18.4mol/L=0.1L��4.6mol/L�����V=0.0250L=25.0mL��
=18.4mol/L��������ҪŨ��������ΪV����V��18.4mol/L=0.1L��4.6mol/L�����V=0.0250L=25.0mL��
(5) A.����Ͳ��ȡŨ����ʱ��������Ͳ�Ŀ̶ȣ�����ȡ��Ũ����ƫ�࣬���ʵ����ʵ���ƫ�������Ƶ���ҺŨ��ƫ�ߣ�A���������⣻
B.����ƿδ���T����������Һ����Ӱ����Һ�����ƣ���˶����Ƶ���ҺŨ����Ӱ�죬B���������⣻
C.Ũ�������ձ���ϡ�ͺ�δ��ȴ������ת�Ƶ�����ƿ�У������ж��ݣ�����Һ�ָ�������ʱ����Һ�����ƫС���������Ƶ���ҺŨ��ƫ�ߣ�C���������⣻
D.������ƿת��ʱ��������Һ�彦�����������ʵ����ʵ���ƫ�٣�ʹ���Ƶ���Һ��Ũ��ƫ�ͣ�D�������⣻
E.ϴ����Ͳ�е�Һ��ע���ձ����������ʵ����ʵ���ƫ��ʹ���Ƶ���ҺŨ��ƫ�ߣ�E���������⣻
F.�ձ�δ����ϴ�ӣ�ʹ������ʧ�����ʵ����ʵ���ƫ�٣��������Ƶ���ҺŨ��ƫС��F�������⣻
G.���ݺ�����ƿ������ҡ�ȣ����ú�Һ�治���̶��ߣ��ټ�ˮ���̶��ߣ���Һ�����ƫ�������Ƶ���ҺŨ��ƫС��G�������⣻
�ʺ���ѡ����DFG��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤����ʵ�����Ʊ��õ���Cl2�л����HCl����ͬѧ�������ͼ��ʾ��ʵ��װ�ã���Ҫ��ش��������⡣

��1������ݼ�ͬѧ��ʾ��ͼ������ʵ��װ�ô������ҵ�����˳��װ�â���__________��
��2��װ�â�����Ҫ��������������__________��__________��__________��
��3��ʵ�����Ʊ�Cl2�����ӷ���ʽΪ____________��
��4��װ�â���Cu������__________���û�ѧ����ʽ��ʾ����
��5����ͬѧ��Ϊ��ͬѧʵ�������Ȼ����ȱ�ݣ�����֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�Ϊ�ˣ���ͬѧ�������ͨ��װ�â�֮ǰ��Ҫ��װһ������װ�âݣ���֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�����Ϊװ�â�Ӧ����__________��
��6����ͬѧ������ͬѧ��Ƶ�װ�ú����������װ�ã�ֻ�轫ԭ���ձ��е�AgNO3��Һ������ɫʯ����Һ������۲쵽__________��������֤����Cl2ʱ��HCl�ӷ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�����ת��������ͼ��ʾ�����з�����������
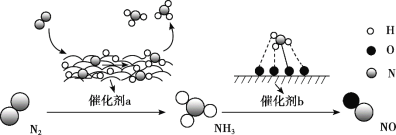
A. ����a���淢���˼��Թ��ۼ��Ķ��Ѻ��γ�
B. N2��H2��Ӧ����NH3��ԭ��������Ϊ100%
C. �ڴ���b�����γɵ�����ʱ�����漰����ת��
D. ����a��b����߷�Ӧ��ƽ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���������л�ѧ��Ӧ��ʵ�������Ʊ��������������й��������ʵ��о���
![]()
(1)��С��ͬѧ����ͼ��ʾ�������Լ�(��һ��ȫ��)�Ʊ����ռ������������������

�� Ӧ��ѡ���������__________(����ĸ)��
�� �����������Ⱥ�˳����������,Ӧ����a��__________��__________��__________��__________��__________��__________��h(�õ��ܿڴ�����ĸ��ʾ)��
�� Ũ������������̷�Ӧ�����ӷ���ʽΪ__________��
(2)��С��ͬѧ��Ʒֱ�����ͼ��ʾװ��̽�������������ԡ�
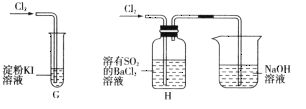
��G�е�������__________��ԭ����__________(�û�ѧ����ʽ��ʾ)��
��H�������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϵ�ⱥ��ʳ��ˮ��ȡ�����Ļ�ѧ����ʽ���£�2NaCl+2H2O![]() 2NaOH+H2��+Cl2�������б�ʾ��Ӧ��������Ļ�ѧ������ȷ���ǣ�������
2NaOH+H2��+Cl2�������б�ʾ��Ӧ��������Ļ�ѧ������ȷ���ǣ�������
A.Na+�Ľṹʾ��ͼ��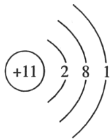
B.������Ϊ18����ԭ�ӣ�![]() Cl
Cl
C.NaOH�ĵ���ʽ��![]()
D.Cl2�Ľṹʽ��Cl��Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪AΪ�����Ľ������ʣ�������ͼ��ʾ�Ĺ�ϵ��

��1��ȷ��A��B��C��D��E��F�Ļ�ѧʽ��AΪ________��BΪ________��CΪ________��DΪ________��EΪ________��FΪ________��
��2��д����Ļ�ѧ����ʽ���ܡ��ݵ����ӷ���ʽ��
��_________________________________________________��
��________________________________________________��
��___________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ����������ʧ����ҩ����ĺϳ�·����ͼ��ʾ��
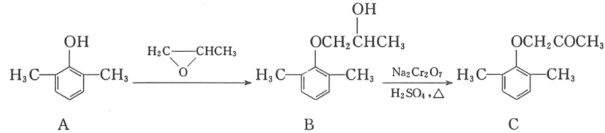
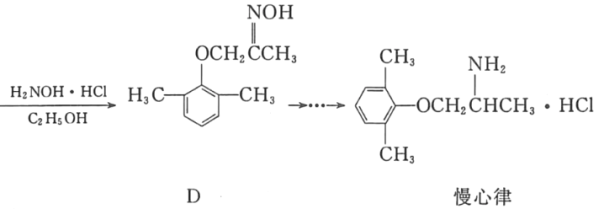
��1��C�еĺ�������������Ϊ_____��_____��
��2����B��C�ķ�Ӧ������_____��
��3����A�Ʊ�B�Ĺ�����������������E������B��Ϊͬ���칹�塣д��E�Ľṹ��ʽ��_____��
��4��д��ͬʱ�������������Ļ�����D��һ��ͬ���칹��Ľṹ��ʽ��_____��
������a����������DZ���������ұ����ϵ�һ�ȴ���ֻ�����֣��۷�������2������̼ԭ��
��5����֪��ϩ�ڴ�����������������Ӧ�������ɻ������飨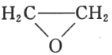 ����д�����ڼ����ӣ�
����д�����ڼ����ӣ� �����Ҵ�Ϊԭ���Ʊ�
�����Ҵ�Ϊԭ���Ʊ�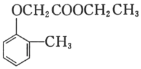 �ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����������_____��
�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��Ԫ�����ڱ��еĶ�����Ԫ�أ����ǵ����λ�����±���ʾ������X��Y Ԫ�ؾ����γ�10���ӵ��⻯�Z��ԭ��������Y��2������ش��������⣺
X | Y | |
Z | W |
(1)W�ļ����ӵĽṹʾ��ͼΪ______��YԪ�������ڱ��е�λ����____��
(2)д��ʵ������WԪ�ص��ʵ����ӷ���ʽ��___________
(3)����Wͬ����Ԫ�أ�����˵����ȷ���ǣ�__________
A.���ϵ����ܶ�������
B.���ϵ����۵�ͷе㶼������
C.���ϵ���Ԫ�صķǽ�����Խ��Խǿ
D.ͬ����Ԫ�ض�Ӧ�ĵ����У�ֻ��WԪ�ض�Ӧ�ĵ����ڳ�̬��Ϊ��̬
(4)W��Z�γɵ�Һ�廯����Z2W2�������ʿ���ˮ��Ӧ����ZO2���壬1 mol Z2W2�μӷ�Ӧʱת��1.5 mol���ӣ�����ֻ��һ��Ԫ�ػ��ϼ۷����ı䣬Z2W2��ˮ��Ӧ�Ļ�ѧ����ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����������ת��������AΪ����������CΪ�

�Իش�
(1)д��F�Ļ�ѧʽ_______________��H�Ļ�ѧʽ___________________��
(2)д����Eת���F�Ļ�ѧ����ʽ��_________________________________��
(3)��G��Һ����A���йط�Ӧ���ӷ���ʽ��____________________��
(4)д��A��һ����������ˮ��Ӧ�Ļ�ѧ����ʽ����˫���ű���÷�Ӧ�ĵ���ת�����__________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com