
| A. | pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合溶液的pH=7,则反应后的混合溶液:2c(R2-)+c(HR-)=c(Na+) | |
| B. | 若将CO2通入0.1mol•L-1 Na2CO3溶液中至溶液中性,则溶液中c(H+)-c(CO32-)=c(OH-)-c(H2CO3) | |
| C. | 将c mol•L-1 的醋酸溶液与0.02mol•L-1 NaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示醋酸的电离常数Ka=$\frac{2×1{0}^{-9}}{c-0.02}$ | |
| D. | 物质的量浓度之比为1:1的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(CO32-) |
分析 A.常温下,pH=3的二元弱酸H2R溶液中酸的物质的量浓度大于0.01mol/L,pH=11的NaOH溶液中氢氧化钠的物质的量浓度是0.01mol/L,混合溶液呈中性,说明溶液中c(OH-)=c(H+),根据电荷守恒和物料守恒分析解答;
B.依据反应过程和溶液中存在的电荷守恒分析判断;
C.呈中性则c(H+)=c(OH-)=10-7mol/L,c(Na+)=c(CH3COO-)=0.01mol/L,以此计算;
D.等物质的量NaClO和NaHCO3的混合液中,由物料守恒可知,n(Na)=n(Cl)+n(C);
解答 解:A.混合溶液呈中性,则c(OH-)=c(H+),根据电荷守恒知,(Na+)+c(H+)=c(OH-)+2(R2-)+c(HR-),所以2c(R2-)+c(HR-)=c(Na+),故A正确;
B.将CO2通入①溶液中恰好呈中性,溶液中存在电荷守恒,c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(HCO3-),c(H+)=c(OH-),则得到c(Na+)=2c(CO32-)+c(HCO3-)=0.2mol/L,选项中若溶液中c(H+)-c(CO32-)=c(OH-)-c(H2CO3),c(CO32-)=c(H2CO3),此时溶液显碱性,故B错误;
C.呈中性则c(H+)=c(OH-)=10-7mol/L,c(Na+)=c(CH3COO-)=0.01mol/L,所以用含c的代数式表示CH3COOH的电离常数Ka=$\frac{1{0}^{-7}×0.01}{\frac{c}{2}-0.01}$=$\frac{2×1{0}^{-9}}{c-0.02}$mol•L-1,故C正确;
D.等物质的量NaClO和NaHCO3的混合液中,由物料守恒可知,n(Na)=n(Cl)+n(C),则[Na+]=[ClO-]+[HClO]+[HCO3-]+[HCO32-]+[H2CO3],故D错误;
故选AC.
点评 本题考查盐类水解的应用,为高频考点,侧重于学生的分析能力的考查,明确盐类水解规律及酸性强弱的关系、电离平衡常数的计算,电解质溶液中电荷守恒和物料守恒等即可解答,题目难度中等.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:选择题
 有一种蓝色晶体【可表示为MxFey(CN)6】,经射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上,其晶体中阴离子的最小结构单元如图所示,下列说法正确的是( )
有一种蓝色晶体【可表示为MxFey(CN)6】,经射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上,其晶体中阴离子的最小结构单元如图所示,下列说法正确的是( )| A. | 该晶体的化学式为M2Fe2(CN)6 | |
| B. | 该晶体属于离子晶体,M呈+1价 | |
| C. | 该晶体属于离子晶体,M呈+2价 | |
| D. | 晶体中与每个Fe3+距离最近且等距离的CN-为3个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
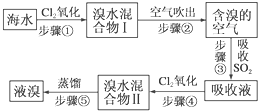
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 | |
| B. | 向某恒容密闭容器中通入1mol SO2和0.5 molO2,达到平衡时放出热量为98.5 kJ | |
| C. | 升高温度能使逆反应速率加快,正反应速率减慢 | |
| D. | 向某恒容密闭容器中通入一定量的SO2和O2达到平衡后,再通入少量气体He,平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能起催化剂的作用 | B. | 受热分解能放出气体 | ||
| C. | 具有净水剂的作用 | D. | 在水中能起到酸的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
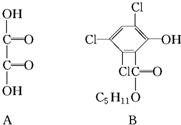 化合物A、B可合成荧光“魔棒”中产生能量的物质之一(CPPO).
化合物A、B可合成荧光“魔棒”中产生能量的物质之一(CPPO).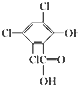 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 向一定量MgCl2、AlCl3溶液中滴加常用试剂NaOH与盐酸(t时刻之前滴加的试剂a,t时刻之后改滴试剂b),沉淀的物质的量y(mol)与试剂体积x(mL)间的关系曲线如图所示.试回答:
向一定量MgCl2、AlCl3溶液中滴加常用试剂NaOH与盐酸(t时刻之前滴加的试剂a,t时刻之后改滴试剂b),沉淀的物质的量y(mol)与试剂体积x(mL)间的关系曲线如图所示.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属镁燃烧后会发出耀眼的白光,因此常用来制造信号弹和焰火 | |
| B. | 金属钠在高温下能将TaCl4中的钛置换出来 | |
| C. | 金属镁着火,可用二氧化碳灭火 | |
| D. | 电解熔融NaCl可以得到金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
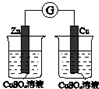 |  | 将等体积的 甲烷和氯气 混合光照 | 5%的H2O2溶 液中滴入2滴 1mol•L-1氯化 铁溶液 |
| 验证化学能 转化为电能 | 验证氧化性Cl2>Br2>I2 | 得到纯净 的一氯甲烷 | 验证催化剂加快 反应速率 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com