
A、
| ||
B、
| ||
C、
| ||
D、
|
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=+28.7kJ/mol |
| B、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-28.7kJ/mol |
| C、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=+57.4kJ/mol |
| D、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁跟盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、碳酸氢钙溶液跟过量氢氧化钠溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、次氯酸钙溶液中通入过量的CO2:ClO-+H2O+CO2=HCO3-+HClO |
| D、氯化铝溶液与过量的氨水反应:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150 mL 1 mol?L-1的NaCl |
| B、75 mL 2 mol?L-1的NH4Cl |
| C、150 mL 3 mol?L-1的KCl |
| D、75 mL 2 mol?L-1的CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、电子式 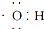 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
B、比例模型  可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 |
C、结构示意图为 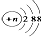 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 |
D、原子结构示意图 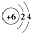 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体积相同,但不一定是22.4L |
| B、分子数相同,但原子数不同 |
| C、摩尔质量不同,但质量相同 |
| D、质子数不同,电子数也不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是表示物质质量的单位 |
| B、摩尔是表示物质微粒数的单位 |
| C、摩尔是表示物质的量的单位 |
| D、摩尔是用来表示原子、分子的质量的单位 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 相关信息 |
| U | 所处的周期数、族序数分别与其原子序数相等. |
| V | 基态时,电子分布在三个能级上,且各能级中电子数相等. |
| W | 基态时,2P轨道处于半充满状态 |
| X | 与W元素处于同一周期,且X第一电离能小于W的第一电离能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com