
科目:高中化学 来源:不详 题型:单选题
| A | B | C | D | |
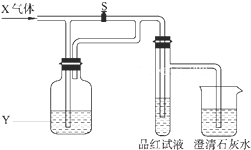
| X | H2S | SO2 | CO2 | Cl2 |
| Y | 浓硫酸 | NaHCO3 饱和溶液 | Na2SO3 溶液 | NaHSO3 饱和溶液 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| O | 2-3 |
| O | 2-4 |
| O | -3 |
| O | 2-3 |
| O | 2-4 |
| O | -3 |
| 步骤编号 | 实验操作 | 预期现象和结论 |
| ① | 用胶头滴管取少量样品溶液加入试管中,再用胶头滴管取过量的1mol?L-1氯化钡溶液并滴加到此试管中,充分反应后,静置,然后过滤,将沉淀和滤液分别装入另外的两个试管中 | 产生白色沉淀 |
| ② | ______ | ______ |
| ③ | ______ | ______ |
| ④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定含有Mg2+、Al3+、Cl-,不含有Na+、NH4+ |
| B.一定含有Na+、Mg2+、Cl-,不含有NH4+、可能含有Al3+ |
| C.c(Mg2+)为1.00mol?L-1,c(Na+)为1.50mol?L-1 |
| D.c(Cl-)为5.00mol?L-1,c(Al3+)为1.00mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入硝酸银溶液时有白色沉淀 |
| B.加入氯化钡溶液时有白色沉淀 |
| C.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失? |
| D.加入足量盐酸无明显现象,再滴加氯化钡溶液有白色沉淀? |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某溶液中加入氯化钡溶液有白色沉淀生成,且沉淀不溶于稀硝酸,则原溶液一定含有SO42- |
| B.某溶液中加入盐酸放出能使澄清的石灰水变浑浊的无色无味的气体,则原溶液一定含有CO32- |
| C.将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L |
| D.同温同压下的一氧化碳气体和氮气,若体积相等,则质量一定相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B.过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C.汽油和水的混合物可用分液的方法分离 |
| D.检验某溶液中是否含有SO42-的方法是先向该溶液中加入BaCl2溶液,再加入稀HNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com