


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol[Ag (NH3)2]OH配合物中含有9NA个σ键 |
| B、标准状况下,22.4L C2H6O中含C-H键5NA |
| C、1mol冰醋酸和lmol乙醇在加热和浓硫酸条件下充分反应生成的水分子数为NA |
| D、KClO3+6HCl═KCl+3Cl2↑+3H2O反应中,生成71g Cl2时,转移的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 4 |
- 2 |
| A、氯化铵与KNH2反应:NH4Cl+KNH2═KCl+2NH3↑ |
| B、二价活泼金属M与液氨反应:M+2NH3═M(NH2)2+H2↑ |
| C、盐酸与MNH反应:2HCl+MNH═MCl2+NH3↑ |
| D、氯化铵与MO反应:2NH4Cl+MO═M(NH2)2+2HCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
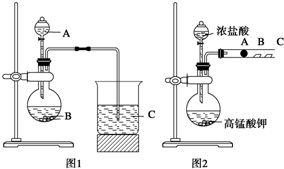 某研究性学习小组设计了一组实验来探究元素周期律.甲同学:根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;
某研究性学习小组设计了一组实验来探究元素周期律.甲同学:根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;查看答案和解析>>
科目:高中化学 来源: 题型:
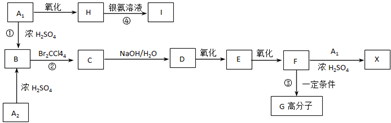
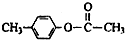 、
、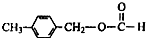 外,其余的结构简式:
外,其余的结构简式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com