
 25 ℃时,浓度均为0.2 mol/L的NaHCO3和Na2CO3溶液中,下列判断不正确的是
25 ℃时,浓度均为0.2 mol/L的NaHCO3和Na2CO3溶液中,下列判断不正确的是
 A. 均存在电离平衡和水解平衡
A. 均存在电离平衡和水解平衡 B. 存在的粒子种类相同
B. 存在的粒子种类相同
 C. c(OH-)前者大于后者
C. c(OH-)前者大于后者 D. 分别加入NaOH固体,恢复到原温度,c(CO32-)均增大
D. 分别加入NaOH固体,恢复到原温度,c(CO32-)均增大
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
常温常压下,下列说法正确的是
A.含有离子键的物质一定是离子化合物 B.同素异形体之间的转化是物理变化
C.含有共价键的物质一定是共价化合物 D.气态物质,其微粒间一定存在共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,回答下列问题:
| 族 周期 | IA | 0 | ||||||
| 一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑨ | ⑥ | ⑦ | ⑧ |
(1)由①、②两种元素组成的相对分子质量为28的有机物的官能团名称为 ,
该物质与溴水发生加成反应的化学方程式是 。
(2)由④、⑤两种元素组成原子个数比为1∶1的物质所含化学键类型为
用电子式表示③的简单氢化物的形成过程: ;
(3)请设计实验比较元素⑥与⑨金属性的相对强弱: ;
(4)由元素②①④按原子个数比为2∶6∶1组成的有机物与④元素的单质可以制成电池,电池中装有KOH浓溶液,将多孔的惰性电极甲和乙浸入KOH溶液中,在甲极通入上述有机物,乙极通入④的单质,则甲极的电极反应式为: 。
(5)由表中①、③、④、⑥、⑧元素形成的常见物质X、Y、Z、M、 N可发生反应(如下图):
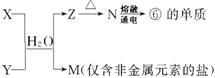
X溶液与Y溶液反应的离子方程式为 ,工业上常用单质⑥冶炼难熔的金属, 写出氧化铁和单质⑥在高温下反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在给定条件下,下列加点的物质在化学反应中完全消耗的是( )
A.用50mL8mol·L-1浓盐酸与10g二氧化锰共热制取氯气
B.标准状况下,将1g铝片投入20mL18.4mol·L-1的硫酸中
C.向100mL3mol·L-1的稀硝酸中加入5.6g铁
D.在5×107Pa、500℃和铁触媒催化的条件下,用氮气和氢气合成氨
查看答案和解析>>
科目:高中化学 来源: 题型:
铁是人类较早使用的金属之一。运用铁的有关知识,回答下列问题:
(1)据有关报道,目前已能冶炼纯度高达99.9999%的铁,关于纯铁的如下叙述中,正确的是( )
A.硬度比生铁高 B.耐腐蚀性强,不易生锈
C.不能与盐酸反应 D.与不锈钢成分相同 E.在冷的浓硫酸中钝化
(2)向沸水中逐滴滴加1mol·L-1FeC13溶液,至液体呈透明的红褐色,形成该分散系的微粒粒度范围是 。
(3)电子工业需用30%的FeC13溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeC13溶液与铜反应的离子方程式 ,检验反应后的溶液中还存在Fe3+的试剂 。
(4)欲从腐蚀后的废液中回收铜并重新获得FeC13溶液,现有下列试剂:①蒸馏水 ②铁粉③浓硝酸④浓盐酸⑤烧碱⑥浓氨水⑦氯气,需要用到的一组试剂是( )
A.①②④⑦ B.①③④⑥ C.②④⑤ D.①④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A. 25℃时NH4Cl溶液的Kw大于100℃时NaCl溶液的Kw
B. SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O SO32―+2I―+4H+
SO32―+2I―+4H+
C. 加入铝粉能产生H2的溶液中,可能存在大量的Na+、Ba2+、AlO2―、NO3-
D. 100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
⑷ 用Al单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式:______________;由R生成Q的化学方程式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.按系统命名法, 的名称为2,7,7-三甲基-3-乙基辛烷
的名称为2,7,7-三甲基-3-乙基辛烷
B.有机物 中,所有原子可能在同一平面上
中,所有原子可能在同一平面上
C. 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4
与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4
D.若两种二肽互为同分异构体,则二者的水解产物一定不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com