
(15分,除标明外,其余每空2分)物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2 2(t-BuNO)
2(t-BuNO)
(1)当(t-BuNO)2的起始浓度(c0)为0.50mol·L-1时,实验测得20℃时的平衡转化率(α)是60%。20℃时上述反应的平衡常数K= 。
(2)一定温度下,随着(t-BuNO)2的起始浓度增大,其平衡转化率 (填“增大”“不变”或“减小”)。已知20℃时该反应在CCl4溶剂中的平衡常数为1.70mol·L-1,若将反应溶剂正庚烷改成CCl4,并保持(t-BuNO)2起始浓度相同,则它在CCl4溶剂中的平衡转化率 (填“大于”“等于”或“小于”)其在正庚烷溶剂中的平衡转化率。
(3)实验测得该反应的ΔH=+50.5kJ·mol-1,活化能Ea=90.4kJ·mol-1。下列能量关系图合理的是 (填字母)。

(4)该反应的ΔS (填“>”“<”或“=”)0。在 (填“较高”或“较低”)温度下有利于该反应自发进行。
(5)通过比色分析得到30℃时(t-BuNO)2浓度随时间的变化关系如图所示,请在同一图中绘出t-BuNO浓度随时间的变化曲线

科目:高中化学 来源:2014-2015学年甘肃省天水市秦安县高三第一次模拟考试化学试卷(解析版) 题型:选择题
下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 检验蔗糖水解产物中的葡萄糖 | 取1 mL 20%蔗糖溶液,加入少量稀硫酸,水浴加热后取少量溶液,加入几滴新制Cu(OH)2,加热 |
B | 除去乙烷中混有的少量乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
C | 验证Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2 mL 1 mol/L NaOH溶液中加入几滴1 mol/L MgCl2溶液,生成白色沉淀,再加入几滴1 mol/L FeCl3溶液 |
D | 硅酸胶体的制备 | 向Na2SiO3溶液(饱和溶液1 : 2用水稀释)中加入几滴酚酞,再逐滴滴入盐酸,边加边振荡,至溶液红色变浅并接近消失 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省皖北协作区高三3月联考理综化学试卷(解析版) 题型:选择题
三聚氯氨是叫种重要的精细化工产品,广泛用于制造农药、染料、炸药、医药等工业。目前工业上生产三聚氯氰的反应原理为:
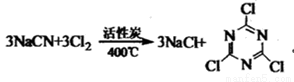
下列有关说法正确的是
A.三聚氯氰中C1的化合价是+1
B.该反应中NaCN被还原
C.三聚氯氰分子中既含 键又含
键又含 健
健
D.36.9 g三聚氯氰中含有1.204×1023个原子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三上学期第一次联考化学试卷(解析版) 题型:填空题
(14分) Ⅰ.已知向含有淀粉的

 酸性溶液滴加
酸性溶液滴加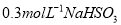 溶液的过程中,溶液的颜色先变蓝色,然后褪色,发生的离子反应如下:
溶液的过程中,溶液的颜色先变蓝色,然后褪色,发生的离子反应如下:
①( ) ( )
( ) =( )
=( ) ( )
( ) ( )
( ) ( )
( )
②
回答下列问题:
(1)写出①反应的离子反应方程式 .
(2)根据①②反应写出还原性粒子 由强到弱的顺序 .
由强到弱的顺序 .
(3)溶液刚好褪色时,则消耗的 溶液的体积为 .
溶液的体积为 .
(4)预测已知向含有淀粉的 溶液滴加
溶液滴加 溶液的现象 .
溶液的现象 .
Ⅱ.在密闭容器中,将碳酸氢钠和过氧化钠的混合粉未加热至250 ,使其充分反应最后测得残余固体中两种化合物的组成分别为
,使其充分反应最后测得残余固体中两种化合物的组成分别为 和
和 ,且
,且 试回答下列问题
试回答下列问题
(1)反应后中固体的成份及其物质的量是: .
(2)原混合物中碳酸氢钠和过氧化钠的物质的量分别为: .
(3)反应后容器气态物质成分及其物质的量是: .
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三上学期第一次联考化学试卷(解析版) 题型:选择题
类推是一种重要的学习方法,但如果不具体问题具体分析就会得出错误的结论,下列类推结论正确的是
A.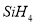 的熔沸点比
的熔沸点比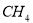 高,则
高,则 的熔沸点比
的熔沸点比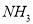 高
高
B.钠在空气中燃烧生成过氧化钠,则锂在空气中燃烧生成过氧化锂
C.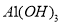 能溶于
能溶于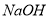 溶液,则
溶液,则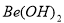 能溶于
能溶于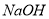 溶液
溶液
D.甲酸甲酯能发生银镜反应,则乙酸甲酯能发生银镜反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三第二次高考模拟化学试卷(解析版) 题型:选择题
下面是生产生活中的常见有机物的分子式结构(简)式或名称:

⑦CH3COOH;⑧硬脂酸甘油酯;⑨蛋白质;⑩聚乙烯。
下列有关说法正确的是
A.能与溴的四氯化碳溶液发生加成反应并使之褪色的有①②④⑩
B.投入钠能产生H2的有⑤⑦⑧⑨
C.属于高分子材料的有⑧⑨⑩
D.含碳量最高有毒常温下为液体且点燃时有浓的黑烟的是①
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:实验题
(15分)硫化碱法是工业上制备硫代硫酸钠晶体(Na2S2O3·5H2O)的方法之一,流程如下:

已知:Na2S2O3在空气中强热会被氧化,Na2S2O3·5H2O在35 ℃以上的干燥空气中易失去结晶水。
(1)甲研究小组设计如下吸硫装置:

①写出A瓶中生成Na2S2O3的化学方程式________________________。
②装置B的作用是检验装置A中SO2的吸收效果,B中试剂可以是________,表明SO2未完全被吸收的实验现象是 。
③为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,可采取的合理措施是 。(写出一条即可)
(2)从滤液中获得较多Na2S2O3·5H2O晶体的实验操作依次为:蒸发浓缩,冷却结晶,过滤,______________,______________。
(3)乙研究小组将二氧化硫气体和氯气同时通入足量氢氧化钠溶液中,小组成员认为吸收液中肯定存在Cl-、OH-和SO42 -,可能存在SO32 -或ClO-。为探究该吸收液中是否存在ClO-,进行了实验研究。请你帮助他们设计实验方案。(限选实验试剂:3 mol·L-1 H2SO4溶液、1 mol·L-1 NaOH溶液、溴水、淀粉KI溶液)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:选择题
下列有关化学用语表达正确的是
A.碳酸氢根离子的水解方程式:HCO3-+H2O H3O++CO32-
H3O++CO32-
B.聚丙烯的结构简式:
C.钾原子的结构示意图: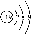
D.甲烷分子的比例模型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com