
| A. | X为0.2 mol•L-1 | |
| B. | Y为0.1 mol•L-1 | |
| C. | Z为0.4 mol•L-1 | |
| D. | Z为0.1 mol•L-1时,Y为0.15 mol•L-1 |
分析 化学平衡的建立,既可以从正反应开始,也可以从逆反应开始,或者从正逆反应开始,不论从哪个方向开始,物质都不能完全反应,利用极限法假设完全反应,计算出相应物质的浓度变化量,实际变化量小于极限值,据此判断分析.
解答 解:若反应向正反应进行,假定完全反应,则:
X2(g)+3Y2(g)?2Z(g)
开始(mol/L):0.1 0.3 0.2
变化(mol/L):0.1 0.3 0.2
平衡(mol/L):0 0 0.4
若反应逆反应进行,假定完全反应,则:
X2(g)+3Y2(g)?2Z(g)
开始(mol/L):0.1 0.3 0.2
变化(mol/L):0.1 0.3 0.2
平衡(mol/L):0.2 0.6 0
由于为可逆反应,物质不能完全转化所以平衡时浓度范围为0<c(X2)<0.2,0<c(Y2)<0.6,0<c(Z)<0.4,故B正确、ACD错误;
故选B.
点评 本题考查化学平衡的建立,关键是利用可逆反应的不完全性,运用极限假设法解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | C3H8只有一种结构 | |
| B. | CH4和CH3CH3是同分异构体 | |
| C. | 组成为C4H10的物质一定是纯净物 | |
| D. | CH3CH2CH2CH3和CH3CH(CH3)2是同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 项目 | 乙炔水化法 | 乙烯氧化法 |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4(催化剂) 100℃~125℃ | PdCl2~CuCl2(催化剂) 100℃~125℃ |
| 平衡转化率 | 乙炔转化率 90% | 乙烯转化率 80% |
| 反应速率 | 较 慢 | 较 快 |
| 原料来源生产工艺 | CaCO3$\stackrel{高温}{→}$CaO$\stackrel{+C电炉}{→}$ CaC2$\stackrel{饱和食盐水}{→}$C2H2 | 石油裂解气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 己烷有4种同分异构体,它们的熔点、沸点各不相同 | |
| B. | 甲醛能发生氧化反应、还原反应和聚合反应 | |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 | |
| D. | 聚合物(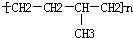 )可由单体CH3CH=CH2和CH2=CH2加聚制得 )可由单体CH3CH=CH2和CH2=CH2加聚制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
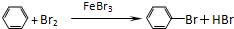
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol•L-1 NH3•H2O溶液与0.1 mol•L-1盐酸等体积混合:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 0.1 mol•L-1 NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 向0.2 mol•L-1 NaHCO3溶液中加入等体积的 0.1 mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1 Na2CO3溶液:c(HCO3-)+c(H2CO3)=c(OH-)-c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其原子核内中子数和质子数都是m | |
| B. | 其原子核内中子数为( n-m )个,核外电子数肯定为n个 | |
| C. | 其原子质量与12C原子质量之比约为n:12 | |
| D. | 其原子质量是12C原子质量的n倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烷烃的同系物的分子式可用通式CnH2n+2表示 | |
| B. | 同系物间具有相似的结构 | |
| C. | 两个同系物之间的相对分子质量差为14或14的整数倍 | |
| D. | 甲烷不是乙炔的同系物,但乙烯是乙炔的同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com