
| A. | x=0.4a,2Fe2++Cl2=2Fe3++2Cl- | |
| B. | x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- | |
| C. | x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| D. | x=0.6a,2Br-+Cl2=Br2+2Cl- |
分析 Fe 2+ 的还原性比Br- 强,所以Cl 2 通入FeBr 2 溶液中,当Cl 2 不足量时,会先与Fe 2+ 反应;待Fe 2+ 全部被氧化成Fe 3+ 后,过量的Cl 2 才会与Br- 反应.
解答 解:由于还原性:Fe2+>Br-,通入Cl2,依次发生2Fe2++Cl2=2Fe3++2Cl-,2Br-+Cl2=Br2+2Cl-,
当n(Cl2):n(FeBr2)≤$\frac{1}{2}$时,只氧化Fe2+,当n(Cl2):n(FeBr2)≥$\frac{3}{2}$时,Fe2+和Br-被完全氧化,介于二者之间时,Fe2+被完全氧化,Br-被部分氧化,则:
A.x=0.4a,n(Cl2):n(FeBr2)=0.4<$\frac{1}{2}$,只氧化Fe2+,故A正确;
B.x=1.5a,Fe2+和Br-恰好被完全氧化,反应的离子方程式为2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-,故B正确;
C.x=a,n(Cl2):n(FeBr2)介于$\frac{1}{2}$~$\frac{3}{2}$,Fe2+被完全氧化,amolFe2+被氧化消耗0.5amolCl2,剩余0.5amolCl2可与amolBr-发生氧化还原反应,则反应的离子方程式为2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-,故C正确;
D.x=0.6a,n(Cl2):n(FeBr2)介于$\frac{1}{2}$~$\frac{3}{2}$,Fe2+被完全氧化,Br-被部分氧化,故D错误;
故选:D.
点评 本题考查了离子方程式书写,侧重考查氧化还原反应离子方程式书写,明确氧化还原反应先后规律,熟悉溴离子、二价铁离子氧化性强弱关系是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在平衡常数表达式中,反应物浓度用起始浓度,生成物用平衡浓度 | |
| B. | 在任何条件下,化学平衡常数是一个恒定值 | |
| C. | 平衡常数的大小只与温度有关,而与浓度、催化剂等无关 | |
| D. | 改变压强,化学平衡常数不一定发生改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
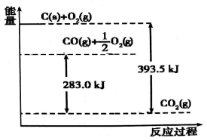
| A. | 1mol C完全燃烧生成CO2时放出的热量为393.5 kJ/mol | |
| B. | 2C(s)+O2(g)═2CO(g)△H=-221.0 kJ/mol | |
| C. | 2CO2 (g)═2CO(g)+O2(g)△H=+283.0 kJ/mol | |
| D. | C(s)+O2(g)═CO2 (g)△H=+393.5 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
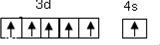 .
.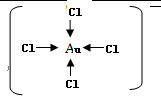 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷没有同分异构体 | |
| B. | CH(CH3)2CH2CH2CH3的一氯代物有4种 | |
| C. | 二氯苯有3种,则四氯苯有6种 | |
| D. | CH3OH与CH2OH-CH2OH都属于醇,互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com